解答题-实验探究题 较难0.4 引用1 组卷287
草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
(1)查阅资料知:草酸晶体175℃分解成CO2、CO、H2O,请写出草酸晶体分解的化学反应方程式:_____ 。
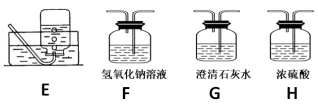
(2)请用下列的装置(图中加热装置已略去)分解草酸晶体以制备少量CO气体,最佳的连接顺序为:________ 。(填字母序号)

(3)设计实验证明草酸为弱酸的方案及其现象均正确的有_____________ (填序号)。
A.室温下,测0.1mol/L的H2C2O4溶液与H2SO4溶液的pH,硫酸溶液的pH比草酸的小;
B.室温下,取pH=3的H2C2O4溶液稀释100倍后,测其pH<5;
C.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL。
(4)现需要配制900mL1mol/L的草酸溶液。
①需要的仪器有托盘天平(带砝码)、钥匙、烧杯、量筒、胶头滴管、_________ 、__________ (填仪器名称)。
②下列操作会使所配溶液浓度偏低的是__________ 。(填字母)
A.称量时用了生锈的砝码
B.容量瓶未干燥即用来配制溶液
C.H2C2O4·2H2O晶体失去了部分结晶水
D.定容时,仰视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(5)用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数)。
①滴定过程中反应的离子方程式为_____________________________________________ 。
②量取KMnO4样品溶液应选用__________ (填“酸式”或“碱式”)滴定管;若量取KMnO4样品溶液的滴定管用蒸馏水洗净后未润洗,则最终的测定结果将________ (填“偏大”、“偏小”或“不变”)。
③现取KMnO4粗品10g,配成100mL溶液,取25.0 mL用(4)中配制的草酸溶液滴定,并进行3次平行实验,所用的草酸溶液的体积分别为23.00 mL、20.02 mL、19.98 mL,请问KMnO4粗品的质量分数为______________ 。(已知:KMnO4的摩尔质量为158g/mol)
(1)查阅资料知:草酸晶体175℃分解成CO2、CO、H2O,请写出草酸晶体分解的化学反应方程式:
(2)请用下列的装置(图中加热装置已略去)分解草酸晶体以制备少量CO气体,最佳的连接顺序为:


(3)设计实验证明草酸为弱酸的方案及其现象均正确的有
A.室温下,测0.1mol/L的H2C2O4溶液与H2SO4溶液的pH,硫酸溶液的pH比草酸的小;
B.室温下,取pH=3的H2C2O4溶液稀释100倍后,测其pH<5;
C.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL。
(4)现需要配制900mL1mol/L的草酸溶液。
①需要的仪器有托盘天平(带砝码)、钥匙、烧杯、量筒、胶头滴管、
②下列操作会使所配溶液浓度偏低的是
A.称量时用了生锈的砝码
B.容量瓶未干燥即用来配制溶液
C.H2C2O4·2H2O晶体失去了部分结晶水
D.定容时,仰视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(5)用草酸滴定KMnO4溶液的方法可测定KMnO4粗品的纯度(质量分数)。
①滴定过程中反应的离子方程式为
②量取KMnO4样品溶液应选用
③现取KMnO4粗品10g,配成100mL溶液,取25.0 mL用(4)中配制的草酸溶液滴定,并进行3次平行实验,所用的草酸溶液的体积分别为23.00 mL、20.02 mL、19.98 mL,请问KMnO4粗品的质量分数为
19-20高三上·广西南宁·阶段练习
类题推荐
草酸是草本植物常具有的成分,具有广泛的用途。草酸晶体(H2C2O4•2H2O)无色易溶于水,熔点为 101 ℃,受热易脱水、升华,在 170 ℃以上分解。常温下,草酸的电离平衡常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
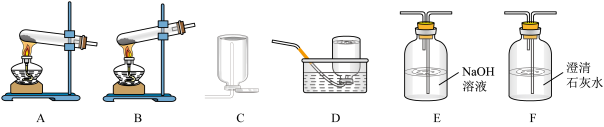
(1)拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为____ (填字母)。
(2)相同温度条件下,分别用 3 支试管按下列要求完成实验:
写出试管 B 中发生反应的离子方程式____________ ;上述实验能否说明“相同条件下,反应物浓度越大,反应速率越快”?_____ (填“能”或“不能”);简述你的理由:__________________ 。
(3)设计实验证明草酸为弱酸的方案及其结果均正确的有________ (填序号)。
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010 mol/L的NaHC2O4溶液,测其pH>7;
C.室温下,取 pH=a(a<3)的H2C2O4溶液稀释100倍后,测其 pH<a+2;
D.取0.10mol/L草酸溶液100mL与足量锌粉反应,收集到H2体积为224mL(标况)。
(4)为测定某H2C2O4溶液的浓度,取20.00 mLH2C2O4溶液于锥形瓶中,滴入2-3滴指示剂,用 0.1000mol/L 的NaOH溶液进行滴定,进行3次平行实验,所用NaOH 溶液体积分别为19.98 mL、20.02 mL 和 22.02mL。
①所用指示剂为__________ ;滴定终点时的现象为________________ ;
②H2C2O4溶液物质的量浓度为________ ;
③下列操作会引起测定结果偏高的是_______ (填序号)。
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.滴定前读数正确,滴定终点时仰视读数
(1)拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为

(2)相同温度条件下,分别用 3 支试管按下列要求完成实验:
| 试管 | A | B | C |
| 4 mL0.01mol/L | 4 mL 0.02mol/L | 4 mL 0.03mol/L | |
| 加入试剂 | KMnO4 | KMnO4 | KMnO4 |
| 1 mL0.1moL/L H2SO4 | 1 mL0.1moL/L H2SO4 | 1 mL0.1moL/LH2SO4 | |
| 2 mL0.1mol/L H2C2O4 | 2 mL 0.1mol/L H2C2O4 | 2 mL 0.1mol/L H2C2O4 | |
| 褪色时间 | 28 秒 | 30 秒 | 不褪色 |
(3)设计实验证明草酸为弱酸的方案及其结果均正确的有
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010 mol/L的NaHC2O4溶液,测其pH>7;
C.室温下,取 pH=a(a<3)的H2C2O4溶液稀释100倍后,测其 pH<a+2;
D.取0.10mol/L草酸溶液100mL与足量锌粉反应,收集到H2体积为224mL(标况)。
(4)为测定某H2C2O4溶液的浓度,取20.00 mLH2C2O4溶液于锥形瓶中,滴入2-3滴指示剂,用 0.1000mol/L 的NaOH溶液进行滴定,进行3次平行实验,所用NaOH 溶液体积分别为19.98 mL、20.02 mL 和 22.02mL。
①所用指示剂为
②H2C2O4溶液物质的量浓度为
③下列操作会引起测定结果偏高的是
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.滴定前读数正确,滴定终点时仰视读数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网