解答题-工业流程题 较难0.4 引用3 组卷207
活性氧化锌是一种多功能性的新型无机材料.某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如下:
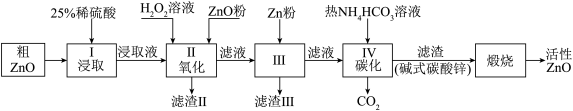
已知各相关氢氧化物沉淀pH范围如下表所示:
完成下列填空:
(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯、量筒外,还需要_____ (选填编号)
A.天平 B.滴定管 C.容量瓶 D.胶头滴管
(2)步骤II中加入H2O2溶液的作用是_________________________ (用离子方程式表示);
(3)用ZnO调节pH,以除去含铁杂质,调节pH的适宜范围是_______________________ 。
(4)步骤III中加入Zn粉的作用是:①__________________ ;②进一步调节溶液pH。
(5)碱式碳酸锌[Zn2(OH)2 CO3]煅烧的化学方程式为________________________________ 。
(6)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):
① 取1.000g活性氧化锌,用15.00mL 1.000mol·L-1 硫酸溶液完全溶解,滴入几滴甲基橙。② 用浓度为0.5000mol·L-1 的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL。判断滴定终点的方法是________ ;所得活性氧化锌的纯度为________ (相对原子质量 O-16 Zn-65 )。

已知各相关氢氧化物沉淀pH范围如下表所示:
| Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
| 完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
完成下列填空:
(1)步骤I中所需25%稀硫酸可用98%浓硫酸(密度为1.84g/mL)配制,所需的仪器除玻璃棒、烧杯、量筒外,还需要
A.天平 B.滴定管 C.容量瓶 D.胶头滴管
(2)步骤II中加入H2O2溶液的作用是
(3)用ZnO调节pH,以除去含铁杂质,调节pH的适宜范围是
(4)步骤III中加入Zn粉的作用是:①
(5)碱式碳酸锌[Zn2(OH)2 CO3]煅烧的化学方程式为
(6)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):
① 取1.000g活性氧化锌,用15.00mL 1.000mol·L-1 硫酸溶液完全溶解,滴入几滴甲基橙。② 用浓度为0.5000mol·L-1 的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL。判断滴定终点的方法是
17-18高二下·四川·期末
类题推荐
活性氧化锌是一种多功能性的新型材料.某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如下:
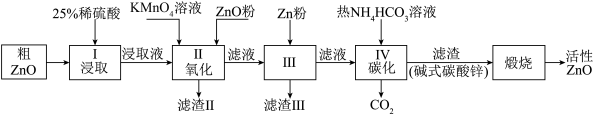
已知各相关氢氧化物沉淀pH范围如下表所示:
(1)步骤II中,在酸性溶液中加入KMnO4的作用是将Fe2+氧化成Fe3+,离子方程式为______________________ ;
(2)用ZnO调节pH,以除去含铁杂质。检验沉淀是否完全的实验操作是________ ;调节pH的适宜范围是____________ 。
(3)步骤III中加入Zn粉的作用是①____________ ,②进一步调节溶液PH值。
(4)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):
取1.000g活性氧化锌,用15.00mL 1.00mol/L硫酸溶液完全溶解,滴入几滴指示剂,再用0.50mol/L的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL,通过计算可以得到活性氧化锌的纯度,由表中Zn(OH)2PH变化可知,滴入的最理想的指示剂是_______ (填“酚酞”、“甲基橙”或“石蕊试剂”)。

已知各相关氢氧化物沉淀pH范围如下表所示:
| Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
| 完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
(1)步骤II中,在酸性溶液中加入KMnO4的作用是将Fe2+氧化成Fe3+,离子方程式为
(2)用ZnO调节pH,以除去含铁杂质。检验沉淀是否完全的实验操作是
(3)步骤III中加入Zn粉的作用是①
(4)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):
取1.000g活性氧化锌,用15.00mL 1.00mol/L硫酸溶液完全溶解,滴入几滴指示剂,再用0.50mol/L的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL,通过计算可以得到活性氧化锌的纯度,由表中Zn(OH)2PH变化可知,滴入的最理想的指示剂是
活性氧化锌是一种多功能性的新型无机材料。某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如图:
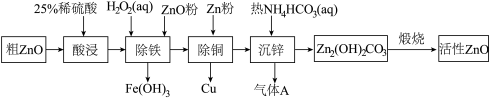
已知相关氢氧化物沉淀pH范围如表所示
下列说法不正确的是( )

已知相关氢氧化物沉淀pH范围如表所示
| Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀 | 5.4 | 7.0 | 2.3 | 4.7 |
| 完全沉淀 | 8.0 | 9.0 | 4.1 | 6.7 |
| A.“酸浸”中25%稀硫酸可用98%浓硫酸配制,需玻璃棒、烧杯、量筒、胶头滴管等仪器 |
| B.“除铁”中用ZnO粉调节溶液pH至4.1~4.7 |
| C.“除铜”中加入Zn粉过量对制备活性氧化锌的产量没有影响 |
| D.“沉锌”反应为2Zn2++4HCO3﹣═Zn2(OH)2CO3↓+3CO2↑+H2O |
活性氧化锌是一种新型多功能无机材料,以粗氧化锌(含铁、铜的氧化物)为原料提纯获得纯净活性氧化锌的生产过程如下:
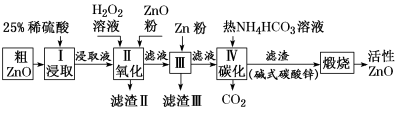
已知各相关氢氧化物沉淀的pH范围如下表所示:
请回答下列问题:
(1)步骤Ⅱ中加入H2O2溶液的作用是_______ (用离子方程式表示)。
(2)用ZnO调节pH,以除去含铁杂质,调节pH的适宜范围是_______ 。
(3)步骤Ⅲ中加入Zn粉的作用:①_______ ;②进一步调节溶液的pH。
(4)碱式碳酸锌[Zn2(OH)2CO3]煅烧的化学方程式为_______ 。

已知各相关氢氧化物沉淀的pH范围如下表所示:
| Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
| 完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
请回答下列问题:
(1)步骤Ⅱ中加入H2O2溶液的作用是
(2)用ZnO调节pH,以除去含铁杂质,调节pH的适宜范围是
(3)步骤Ⅲ中加入Zn粉的作用:①
(4)碱式碳酸锌[Zn2(OH)2CO3]煅烧的化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


