解答题-实验探究题 适中0.65 引用5 组卷241
Ⅰ.实验室常用以下几种方法制取氯气。
(1)二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式_________________________ 。
(2)高锰酸钾与浓盐酸反应制氯气,写出其反应的化学方程式__________________________ 。
(3)氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为________ 。
Ⅱ.某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数的测定。___________ 。
(2)装置③中发生反应的化学方程式为_______________________ ,
该反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是_______________ 。
(3)测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.100 0 mol·L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:
该漂白粉中有效成分的质量分数为________ ;若滴定过程中未充分振荡溶液,局部变浅蓝色时就停止滴定,则测定结果将________ (填“偏高”“偏低”或“无影响”)。
(1)二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式
(2)高锰酸钾与浓盐酸反应制氯气,写出其反应的化学方程式
(3)氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为
Ⅱ.某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数的测定。
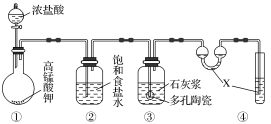
(2)装置③中发生反应的化学方程式为
该反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是
(3)测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.100 0 mol·L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:
3ClO-+I-===3Cl-+IO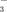
IO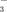 +5I-+3H2O===6OH-+3I2
+5I-+3H2O===6OH-+3I2
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
14-15高三·贵州·阶段练习
类题推荐
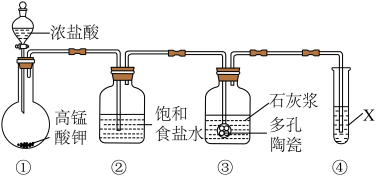
某研究性学习小组利用下列装置制备漂白粉,并测定漂白粉有效成分的质量分数: 试剂为
试剂为___________ 。
【小题2】装置③中发生反应的化学方程式为___________ ,该反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是___________ 。
【小题3】测定漂白粉有效成分的质量分数:称取 漂白粉于锥形瓶中,加水溶解,调节溶液的
漂白粉于锥形瓶中,加水溶解,调节溶液的 ,以淀粉为指示剂,用
,以淀粉为指示剂,用 溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为
溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为 、
、 ,实验测得数据如下表所示:
,实验测得数据如下表所示:
该漂白粉中有效成分的质量分数为___________ ;若滴定过程中未充分振荡溶液,局部变浅蓝色时就停止滴定,则测定结果将___________ (填“偏高”、“偏低”或“无影响”)。
该研究性学习小组再制备饱和氯水,并进行相关的测定:
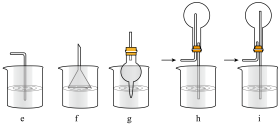
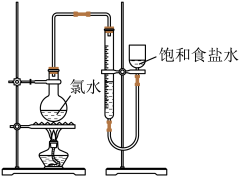
【小题4】为测定饱和氯水中氯元素的总量,某小组设计的实验方案为:使用如图装置,加热 饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是
饱和氯水试样,测定产生气体的体积。此方案不可行的主要原因是___________ 。(不考虑实验装置及操作失误导致不可行的原因) 等物质还原成
等物质还原成 。若要测定饱和氯水中氯元素的总量,需使用的试剂为
。若要测定饱和氯水中氯元素的总量,需使用的试剂为___________ 。
【小题2】装置③中发生反应的化学方程式为
【小题3】测定漂白粉有效成分的质量分数:称取
| 滴定次数 | 1 | 2 | 3 |
| 19.98 | 20.02 | 20.00 |
该研究性学习小组再制备饱和氯水,并进行相关的测定:
【小题4】为测定饱和氯水中氯元素的总量,某小组设计的实验方案为:使用如图装置,加热
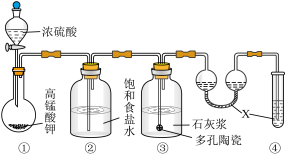
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是________ ,请写出该反应相应的化学方程式: ___________________________________ 。
(2)实验室常用以下几种方法制取氯气。
a.二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式______________ 。
b.氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为____ 。
(3)装置B中饱和食盐水的作用是________ ;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:____________________________ 。
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是________ (填字母编号)。
(5)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是________________ ,该现象________ (填“能”或“不能”)说明溴单质的氧化性强于碘,原因是_________________ 。
(6)装置F的作用是_________ ,其烧杯中的溶液不能选用下列中的________ (填字母编号)。
a.饱和NaOH溶液 b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液
(7)氯气可制漂白粉,测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.100 0 mol/LKI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:3ClO-+I-=3Cl-+IO3-;IO3-+5I-+3H2O=6OH-+3I2,实验测得数据如下表所示。
该漂白粉中有效成分的质量分数为________ ;若滴定过程中未充分振荡溶液,局部变浅蓝色时就停止滴定,则测定结果将________ (填“偏高”“偏低”或“无影响”)。

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是
(2)实验室常用以下几种方法制取氯气。
a.二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式
b.氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为
(3)装置B中饱和食盐水的作用是
(4)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是
(6)装置F的作用是
a.饱和NaOH溶液 b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液
(7)氯气可制漂白粉,测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.100 0 mol/LKI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:3ClO-+I-=3Cl-+IO3-;IO3-+5I-+3H2O=6OH-+3I2,实验测得数据如下表所示。
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
该漂白粉中有效成分的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网