解答题-原理综合题 适中0.65 引用1 组卷684
亚硝酰氧(NOCl)是有机合成中的重要试剂,工业上可由NO与Cl2反应制得,回答下列问题:
(1)NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______
(2)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰气,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g) ΔH1 K1;
NaNO3(s)+NOCl(g) ΔH1 K1;
4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) ΔH2 K2;
2NaNO3(s)+2NO(g)+Cl2(g) ΔH2 K2;
2NO(g)+Cl2(g) 2NOCl(g) ΔH3 K3;
2NOCl(g) ΔH3 K3;
则ΔH3=_____ (用ΔH1和ΔH2表示),K3=______ (用K1和K2表示)
(3)25℃时,向2L带气压计的恒容密闭容器中通入0.08molNO和0.04molCl2发生反应:2NO(g)+Cl2(g)=2NOCl(g) ΔH
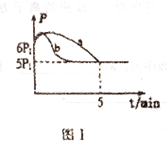
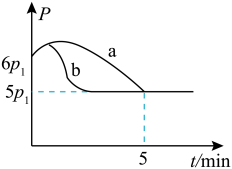
①测得其压强(p)随时间(t)的变化如图I曲线a所示(反应达到平衡时的温度与起始温度相同),则ΔH___ 0 (填“>”或“<”);若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图I曲线b所示,则改变的条件是______ 。
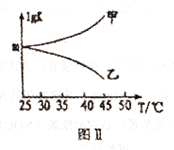
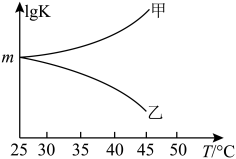
②图Ⅱ是甲、乙同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是______ (填“甲”或“乙”);m值为_______
(4)NO可用间接电化学法除去,其原理如图3所示
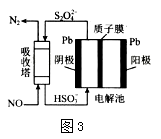
①阴极的电极反应式为_________
②吸收塔内发生反应的离子方程式为___________
(1)NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为
(2)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰气,涉及如下反应:
2NO2(g)+NaCl(s)
 NaNO3(s)+NOCl(g) ΔH1 K1;
NaNO3(s)+NOCl(g) ΔH1 K1;4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g) ΔH2 K2;
2NaNO3(s)+2NO(g)+Cl2(g) ΔH2 K2;2NO(g)+Cl2(g)
 2NOCl(g) ΔH3 K3;
2NOCl(g) ΔH3 K3;则ΔH3=
(3)25℃时,向2L带气压计的恒容密闭容器中通入0.08molNO和0.04molCl2发生反应:2NO(g)+Cl2(g)=2NOCl(g) ΔH
①测得其压强(p)随时间(t)的变化如图I曲线a所示(反应达到平衡时的温度与起始温度相同),则ΔH

②图Ⅱ是甲、乙同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是

(4)NO可用间接电化学法除去,其原理如图3所示

①阴极的电极反应式为
②吸收塔内发生反应的离子方程式为
2018·河北衡水·一模
类题推荐
亚硝酰氯(ClNO)是有机合成中的重要试剂, 工业上可用 NO 与Cl2合成:
(1)一定条件下,氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及反应的热化学方程式和平衡常数如表:
则Δ H3=___________ (用Δ H1、Δ H2表示); K3=___________ (用 K1、K2表示)。
(2)300℃时,在一密闭容器中发生反应:2ClNO(g) 2NO(g)+Cl2 (g),其正反应速率表达式
2NO(g)+Cl2 (g),其正反应速率表达式 正=k·Cn(ClNO)。测得正反应速率和对应浓度的数据如表:
正=k·Cn(ClNO)。测得正反应速率和对应浓度的数据如表:
则n=___________ ,k=___________ 。
(3)25℃时,向体积为2L且带气压计的恒容密闭容器中通入 0.08mol NO 和 0.04mol Cl2,发生反应: 2NO(g)+Cl2 (g) 2ClNO(g) Δ H。
2ClNO(g) Δ H。

已知:反应起始和平衡时温度相同。
①测得反应过程中压强(p)随时间(t)的变化如图曲线 a 所示,则Δ H___________ 0(填“>”“<” 或“不确定”);若其他条件相同,仅改变某一条件时,测得压强(p)随时间(t)的变化如图曲线b所示,则改变的条件是___________ 。
②求该温度下反应的压强平衡常数Kp,写出计算过程___________ 。(注:用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(1)一定条件下,氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及反应的热化学方程式和平衡常数如表:
| 反应 | 热化学方程式 | 平衡常数 |
| ① | 2NO2(g)+ NaCl(s) | K1 |
| ② | 4NO2(g)+ 2NaCl(s) | K2 |
| ③ | 2NO(g)+ Cl2(g) | K3 |
(2)300℃时,在一密闭容器中发生反应:2ClNO(g)
| 序号 | c(ClNO)/(mol ·L-1) | |
| ① | 0.30 | 3.60×10−9 |
| ② | 0.60 | 1.44×10−8 |
| ③ | 0.90 | 3.24×10−8 |
(3)25℃时,向体积为2L且带气压计的恒容密闭容器中通入 0.08mol NO 和 0.04mol Cl2,发生反应: 2NO(g)+Cl2 (g)

已知:反应起始和平衡时温度相同。
①测得反应过程中压强(p)随时间(t)的变化如图曲线 a 所示,则Δ H
②求该温度下反应的压强平衡常数Kp,写出计算过程
亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g)  2NOCl(g)。
2NOCl(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g) K1
NaNO3(s)+NOCl(g) K1
②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g) 2NOCl(g) K3
2NOCl(g) K3
反应①②③对应的平衡常数依次为K1、K2、K3,则K3与K1、K2之间的关系为_________ 。
(2)300℃时,2NOCl(g) 2NO(g)+Cl2(g)。正反应速率的表达式为v正=k·cn(NOCl)(k为
2NO(g)+Cl2(g)。正反应速率的表达式为v正=k·cn(NOCl)(k为带有单位 的速率常数,其值只与温度有关),测得速率与浓度的关系如表所示:
n=_________ ,k=_________ 。
(3)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入一定量NO和 Cl2合成NOCl,方程式为2NO(g)+Cl2(g) 2NOCl(g) △H 若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图1曲线a所示,则 △H
2NOCl(g) △H 若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图1曲线a所示,则 △H _________ (填“>”“<”或“不确定”)0;若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图1曲线b所示,则改变的条件是_________ 。
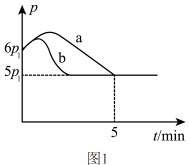
(4)若把2molNO和1molCl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图2所示,若反应一直保持在p压强条件下进行,则M点的分压平衡常数Kp=_________ (用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。

(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s)
②4NO2(g)+2NaCl(s)
③2NO(g)+Cl2(g)
反应①②③对应的平衡常数依次为K1、K2、K3,则K3与K1、K2之间的关系为
(2)300℃时,2NOCl(g)
| 序号 | c(NOCl)/mol·L-1 | v正/mol·L-1·s-1 |
| ① | 0.30 | 3.60×10-9 |
| ② | 0.60 | l.44×10-8 |
| ③ | 0.90 | 3.24×10-8 |
(3)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入一定量NO和 Cl2合成NOCl,方程式为2NO(g)+Cl2(g)

(4)若把2molNO和1molCl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图2所示,若反应一直保持在p压强条件下进行,则M点的分压平衡常数Kp=

亚硝酰氯(ClNO)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g) 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:① 2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s)
NaNO3(s)+ClNO(g) K1;②4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) K2;③2NO(g)+Cl2(g) 2ClNO(g) K3,则K1、K2、K3之间的关系为K3=
2ClNO(g) K3,则K1、K2、K3之间的关系为K3=_______________ (用K1和K2表示);
(2)已知几种化学键的键能数据如下表:(亚硝酰氯的结构为Cl—N==O)
则2NO(g)+Cl2(g) 2ClNO(g)的反应的 △H和a的关系为 △H =
2ClNO(g)的反应的 △H和a的关系为 △H = ___ kJ·mol-1。
(3)300℃时,2NO(g)+Cl2 (g) 2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正 = k·cn (ClNO),测得速率和浓度的关系如下表:
n = ___ ;k = ____ 。
(4)若向绝热恒容密闭容器中充入物质的量之比为2 : 1的NO和Cl2进行反应2NO(g)+Cl2(g) 2ClNO(g),能判断反应已达到化学平衡状态的是
2ClNO(g),能判断反应已达到化学平衡状态的是__ (填标号)。
a.容器中的压强不变 b.2v正(NO) = v逆(Cl2)c.气体的平均相对分子质量保持不变 d.该反应平衡常数保持不变e.NO和Cl2的体积比保持不变
(5)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol NO和0.04 mol Cl2发生反应:2NO(g)+Cl2 (g) 2ClNO(g)△H。
2ClNO(g)△H。
①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图甲曲线a所示,则 △H__ (填“>”“<”或“不确定”)0;若其他条件相同,仅改变某一条件时,测得其压强(p)随时间(t)的变化如图甲曲线b所示,则改变的条件是______ 。
②图是甲、乙同学描绘上述反应平衡常数的对数值(lg K)与温度的变化关系,其中正确的曲线是____ (填“甲”或“乙”),m值为_____ 。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:① 2NO2(g)+NaCl(s)
(2)已知几种化学键的键能数据如下表:(亚硝酰氯的结构为Cl—N==O)
| 化学键 | N≡O | Cl-Cl | Cl-N | N==O |
| 键能/(kJ·mol-1) | 630 | 243 | a | 607 |
(3)300℃时,2NO(g)+Cl2 (g)
| 序号 | c(ClNO)/(mol·L-1) | v/(mol·L-1·s-l) |
| ① | 0. 30 | 3. 60×10-9 |
| ② | 0. 60 | 1. 44×10-8 |
| ③ | 0. 90 | 3. 24×10-8 |
(4)若向绝热恒容密闭容器中充入物质的量之比为2 : 1的NO和Cl2进行反应2NO(g)+Cl2(g)
a.容器中的压强不变 b.2v正(NO) = v逆(Cl2)c.气体的平均相对分子质量保持不变 d.该反应平衡常数保持不变e.NO和Cl2的体积比保持不变
(5)25℃时,向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol NO和0.04 mol Cl2发生反应:2NO(g)+Cl2 (g)
①若反应起始和平衡时温度相同,测得反应过程中压强(p)随时间(t)的变化如图甲曲线a所示,则 △H
②图是甲、乙同学描绘上述反应平衡常数的对数值(lg K)与温度的变化关系,其中正确的曲线是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


