填空题 较难0.4 引用1 组卷340
现有a~i 9种短周期元素,它们在同期表中的位置如下,请据此回答下列问题:(请用具体的元素符号及化学用语作答)
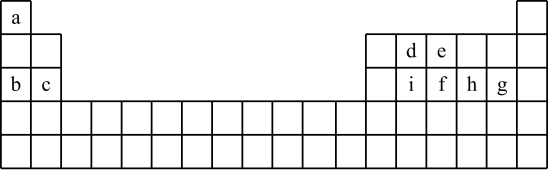
(1)a~i元素中,金属性最强的是________ ,最高价氧化物对应水化物中,酸性最强的物质是___________ 。g所在族的元素形成的氢化物中沸点最低的是____________________ 。
(2)比较b、e、g简单离子半径的大小___________________ (用离子符号作答)。
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式__________________ 、___________________ 。
(4)用一个化学反应方程式表示d的非金属性强于i_______________________________ 。
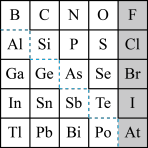
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是______ (填序号)。
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号_________ ;镓(Ga)与As同周期,最外层有3个电子,Ga与As可以形成一种新型化合物半导体材料,其性能更优越。这种新型化合物化学式为____________________ 。
(6)c与a形成的化合物的电子式为___________ ,用电子式表示a与h形成a2h的过程__________________________________________ 。
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式_________________________________ 。

(1)a~i元素中,金属性最强的是
(2)比较b、e、g简单离子半径的大小
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式
(4)用一个化学反应方程式表示d的非金属性强于i
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号
(6)c与a形成的化合物的电子式为
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式
17-18高一下·重庆·期中
类题推荐
A、B、C、D、E是五种短周期主族元素,已知:
①B是地壳中含量最多的金属元素;
②A、B、E在同一周期,在该周期所有主族元素中,A的原子半径最大,E的原子半径最小;
③ 、
、 具有相同的电子层结构;
具有相同的电子层结构;
④热稳定性: 。
。
根据上述信息回答下列问题:
(1)D在元素周期表中的位置为_________ 。
(2) 的电子式为
的电子式为_________ 。
(3)A、B、C、D四种元素的简单离子半径由大到小的顺序为_________ (用离子符号表示,下同)。
(4) 、
、 的还原性强弱顺序为
的还原性强弱顺序为_________ 。
(5) 与C元素的具有漂白性的氧化物反应的化学方程式为
与C元素的具有漂白性的氧化物反应的化学方程式为_________ 。
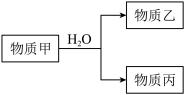
(6)在A、B、C、E形成的单质中,符合下列转化关系的是_________ (填元素符号)。

(7)镓(Ga)与B同主族且相邻,性质相似。金属镓在半导体材料等领域具有重要应用。下列有关镓和镓的化合物说法正确的是_________(填字母)。
①B是地壳中含量最多的金属元素;
②A、B、E在同一周期,在该周期所有主族元素中,A的原子半径最大,E的原子半径最小;
③
④热稳定性:
根据上述信息回答下列问题:
(1)D在元素周期表中的位置为
(2)
(3)A、B、C、D四种元素的简单离子半径由大到小的顺序为
(4)
(5)
(6)在A、B、C、E形成的单质中,符合下列转化关系的是

(7)镓(Ga)与B同主族且相邻,性质相似。金属镓在半导体材料等领域具有重要应用。下列有关镓和镓的化合物说法正确的是_________(填字母)。
| A.一定条件下, |
| B.常温下, |
| C. |
| D.一定条件下, |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网