单选题 适中0.65 引用3 组卷754
Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4,下列有关说法不正确的是


| A.右侧电极反应方程式:Fe+8OH--6e-=FeO42-+4H2O |
| B.左侧为阳离子交换膜,当Cu电极生成1mol气体时,有2molNa+通过阳离子交换膜 |
| C.可以将左侧流出的氢氧化钠补充到该装置中部,以保证装置连续工作 |
| D.Na2FeO4具有强氧化性且产物为Fe3+,因此可以利用Na2FeO4除去水中的细菌、固体颗粒以及Ca2+等 |
2018·河南·二模
类题推荐  是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产
是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产 ,下列有关说法不正确的是
,下列有关说法不正确的是
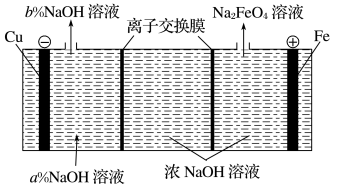

| A.右侧电极反应方程式: |
| B.左侧为阳离子交换膜,右侧为阴离子交换膜 |
| C.阴极生成 |
| D. |
Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4,下列说法正确的是
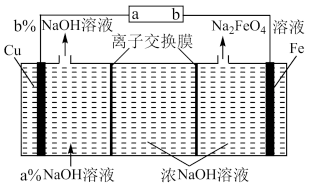

| A.电源a极为正极 |
| B.阴极区a%>b% |
| C.阳极的电极反应式为Fe-6e-+8OH-=FeO |
| D.每产生1molNa2FeO4,有8molNa+通过左侧离子交换膜 |
电化学原理在工业生产中发挥着巨大的作用。Na2FeO4是制造高铁电池的重要原料,同时也是一种新型的高效净水剂。在工业上通常利用如图装置生产Na2FeO4,下列说法正确的是
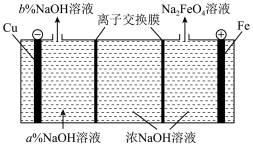
| A.阳极的电极反应式为Fe+8OH--6e-=FeO |
| B.右侧的离子交换膜为阳离子交换膜 |
| C.阴极区a%>b% |
| D.阴极产生的气体是氧气 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


