解答题-结构与性质 适中0.65 引用1 组卷205
氮、磷、砷是第VA族的元素,它们的单质及其化合物在生产生活中均有重要作用。请回答以下问题:
(1) 基态砷原子的最外层电子排布式为______ ;有_____ 个能级。
(2) N、P、As原子的第一电离能由大到小的顺序为________ 。
(3) 氮元素的一种重要化合物尿素CO(NH2)2分子中,σ键和π键的数目之比为______ 。
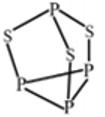
(4) P4S3 可用于制造火柴,其分子结构如图所示,判断P4S3 分子中硫原子的杂化轨道类型为_____ ,每个P4S3 分子中含孤电子对的数目为_______ 。
(5) Na3AsO4 可用作杀虫剂,AsO43-的空间构型为_______ ,与AsO43-互为等电子体的一种分子为_____ (填写化学式)。
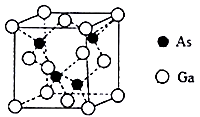
(6) ①砷化镓(GaAs) 为黑灰色固体,熔点为1238℃,其晶胞结构如图所示。该晶体属于____ 晶体,微粒之间存在的作用力是_______ 。
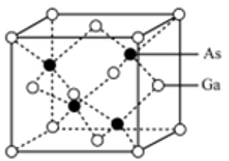
② 砷化镓晶胞中距离Ga原子等距且最近的Ga原子有______ 个,已知砷化镓晶胞边长为apm,其密度为ρg·cm-3,则阿伏伽德罗常数的值_______ (列出计算式即可)。
(1) 基态砷原子的最外层电子排布式为
(2) N、P、As原子的第一电离能由大到小的顺序为
(3) 氮元素的一种重要化合物尿素CO(NH2)2分子中,σ键和π键的数目之比为
(4) P4S3 可用于制造火柴,其分子结构如图所示,判断P4S3 分子中硫原子的杂化轨道类型为

(5) Na3AsO4 可用作杀虫剂,AsO43-的空间构型为
(6) ①砷化镓(GaAs) 为黑灰色固体,熔点为1238℃,其晶胞结构如图所示。该晶体属于

② 砷化镓晶胞中距离Ga原子等距且最近的Ga原子有
2018·贵州安顺·一模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网