解答题-结构与性质 适中0.65 引用3 组卷200
科学家正在研究温室气体CH4和CO2的转化和利用。请回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_______ 形象化描述。在基态14C原子中,核外存在_______ 对自旋相反的电子。
(2)CH4和CO2所含的三种元素电负性从小到大的顺序为_______ 。
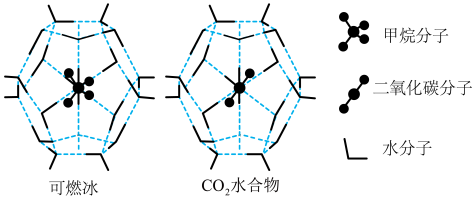
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。

①下列关于CH4和CO2的说法正确的是_______ (填序号)。
a.CO2分子中含有2个σ键和2个π键
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表所提供的数据分析,提出该设想的依据是_______ 。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)CH4和CO2所含的三种元素电负性从小到大的顺序为
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。
| 参数 分子 | 分子直径/nm | 分子与H2O的结合能E/kJ·mol-1 |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |

①下列关于CH4和CO2的说法正确的是
a.CO2分子中含有2个σ键和2个π键
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表所提供的数据分析,提出该设想的依据是
17-18高二下·山东·期中
类题推荐
我国可燃冰资源一直被视为能源领域的宝藏,可燃冰被寄予厚望成为替代传统石油和天然气的清洁能源。回答下列问题:
(1)一定条件下, 、
、 都能与
都能与 形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。
形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。 与
与 形成的水合物晶体俗称“可燃冰”。
形成的水合物晶体俗称“可燃冰”。
 和
和 所含的三种元素电负性从大到小的顺序为
所含的三种元素电负性从大到小的顺序为___________ ;碳原子的最高能级的符号是___________ ,其电子云形状是___________ 。
(2) 分子的空间结构为
分子的空间结构为___________ 。相同条件下 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是 ,理由是
,理由是___________ 。
(3)“可燃冰”中分子间存在的两种作用力是___________ 。
(4)下列关于 和
和 的说法正确的是___________(填标号)。
的说法正确的是___________(填标号)。
(5)为开采深海海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________ 。
(1)一定条件下,
| 参数分子 | 分子直径/nm | 分子与 |
| 0.436 | 16.40 | |
| 0.512 | 29.91 |
(2)
(3)“可燃冰”中分子间存在的两种作用力是
(4)下列关于
| A. |
| B. |
| C.因为碳氢键键能小于碳氧键,所以 |
| D. |
(5)为开采深海海底的“可燃冰”,有科学家提出用
含碳物质广泛存在于有机物和无机物中。回答下列问题:
(1)基态C原子的未成对电子数为___________ 。
(2)科学家正致力于研究温室气体CH4和CO2的转化和利用。
①下列有关CH4和CO2的说法正确的是___________ (填标号)。
a.两者都为含有极性共价键的极性分子
b.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
c.CH4与SiH4互为等电子体,故SiO2与CO2互为等电子体
d.电负性大小:O>C>H
一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。

②“可燃冰”中分子间存在的2种作用力是___________ 。
③为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586 nm,结合图表从物质结构及性质的角度分析,该设想的依据是:___________ 。
(3)发现C60的三位科学家荣获了1996年的诺贝尔化学奖。
①C60的分子结构如图所示,则1 mol C60分子含有的σ键的数目为___________ 。

②根据理论计算,C60中碳原子的杂化方式既不是sp2,也不是sp3,而是介于两者之间的sp2.28.据此推测,下列球碳(碳原子彼此链接形成类似C60的球形结构)中的碳原子的杂化方式,最接近sp2杂化的是___________ 。
a.C20 b.C80 c.C240 d.C540
③C60分子中成键方式可视为每个原子接2个单键和1个双键,它能与F2发生加成反应,其加成产物为___________ 。
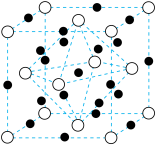
④C60与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。K与C60形成的一种超导材料的晶胞如图所示,图中白球表示C60,黑球表示钾原子。该材料的化学式为___________ 。已知晶胞边长为a=1424 pm,则该超导材料的理论密度ρ的计算式为___________ 。
(1)基态C原子的未成对电子数为
(2)科学家正致力于研究温室气体CH4和CO2的转化和利用。
①下列有关CH4和CO2的说法正确的是
a.两者都为含有极性共价键的极性分子
b.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
c.CH4与SiH4互为等电子体,故SiO2与CO2互为等电子体
d.电负性大小:O>C>H
一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。

| 参数分子 | 分子直径/nm | 分子与H2O的结合能 E/(kJ·mol-1) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
③为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586 nm,结合图表从物质结构及性质的角度分析,该设想的依据是:
(3)发现C60的三位科学家荣获了1996年的诺贝尔化学奖。
①C60的分子结构如图所示,则1 mol C60分子含有的σ键的数目为

②根据理论计算,C60中碳原子的杂化方式既不是sp2,也不是sp3,而是介于两者之间的sp2.28.据此推测,下列球碳(碳原子彼此链接形成类似C60的球形结构)中的碳原子的杂化方式,最接近sp2杂化的是
a.C20 b.C80 c.C240 d.C540
③C60分子中成键方式可视为每个原子接2个单键和1个双键,它能与F2发生加成反应,其加成产物为
④C60与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。K与C60形成的一种超导材料的晶胞如图所示,图中白球表示C60,黑球表示钾原子。该材料的化学式为

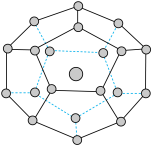
2017年5月海底天然气水合物(俗称可燃冰)试采成功,这是我国能源开发的一次历史性突破。一定条件下,CH4和CO2都能与H2O形成如图所示的笼状结构(表面的小球是水分子,内部的大球是CH4分子或CO2分子;“可燃冰”是CH4与H2O形成的水合物),其相关参数见下表。
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为___________ ;碳原子的最高能级的符号是___________ ,其电子云形状是___________ 。
(2) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为___________ ,分子的空间结构为___________ 。
(3)为开采海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知图中笼状结构的空腔直径为
的设想。已知图中笼状结构的空腔直径为 ,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________ 。
(4)“可燃冰”中分子间存在的作用力是氢键和___________ ,上图中最小的环中连接的原子总数是___________ 。
| 参数分子 | 分子直径/nm | 分子与H2O的结合能E(kJ·mol-1) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
(1)CH4和CO2所含的三种元素电负性从大到小的顺序为
(2)
(3)为开采海底的“可燃冰”,有科学家提出用
(4)“可燃冰”中分子间存在的作用力是氢键和
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


