解答题-原理综合题 较难0.4 引用1 组卷330
金属钒被誉为“合金的维生素”,常用于催化剂和新型电池。钒(V)在溶液中主要以VO43-(黄色)、VO2+(浅黄色)、VO2+ (蓝色)、V3+(绿色)、V2+(紫色)等形式存在。回答下列问题:
(1)已知:4Al(s)+3O2(g)=2Al2O3(s) △H1 4V(s)+5O2(g)=2V2O5(s) △H2
写出V2O5与Al 反应制备金属钒的热化学方程式__________________ 。(反应热用△H1、△H2表示)
(2) V2O5具有强氧化性,溶于浓盐酸可以得到蓝色溶液(含有VO2+),试写出V2O5与浓盐酸
反应的化学反应方程式:_________________________________ 。
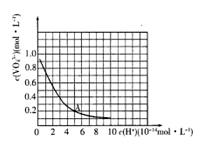
(3)VO43-和V2O74-在pH≥13的溶液中可相互转化。室温下,1.0mol·L-1的Na3VO4溶液中c(VO43-)随c(H+)的变化如图所示。溶液中c(H+)增大,VO43-的平衡转化率_________ (填“增大”“减小”或“不变”)。根据A点数据,计算该转化反应的平衡常数的数值为________ 。
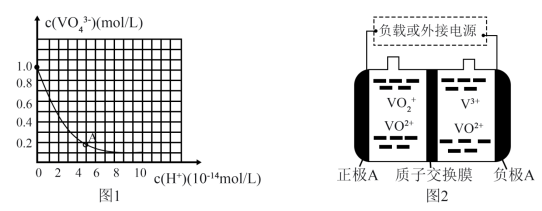
(4)全钒液流电池是一种优良的新型蓄电储能设备,其工作原理如图2所示:
①放电过程中,A电极的反应式为___________________ 。
②充电过程中,B电极附近溶液颜色变化为___________________ 。
③若该电池放电时的电流强度I=2.0A,电池工作10分钟,电解精炼铜得到铜mg,则电流利用率为______________ (写出表达式,不必计算出结果。已知:电量Q=It,t为时间/秒;电解时Q=znF,z为每摩尔物质得失电子摩尔数,n为物质的量,法拉第常数F=96500C/mol,电流利用效率= ×100%)
×100%)
(1)已知:4Al(s)+3O2(g)=2Al2O3(s) △H1 4V(s)+5O2(g)=2V2O5(s) △H2
写出V2O5与Al 反应制备金属钒的热化学方程式
(2) V2O5具有强氧化性,溶于浓盐酸可以得到蓝色溶液(含有VO2+),试写出V2O5与浓盐酸
反应的化学反应方程式:
(3)VO43-和V2O74-在pH≥13的溶液中可相互转化。室温下,1.0mol·L-1的Na3VO4溶液中c(VO43-)随c(H+)的变化如图所示。溶液中c(H+)增大,VO43-的平衡转化率

(4)全钒液流电池是一种优良的新型蓄电储能设备,其工作原理如图2所示:
①放电过程中,A电极的反应式为
②充电过程中,B电极附近溶液颜色变化为
③若该电池放电时的电流强度I=2.0A,电池工作10分钟,电解精炼铜得到铜mg,则电流利用率为
2018·广东珠海·一模
类题推荐
为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
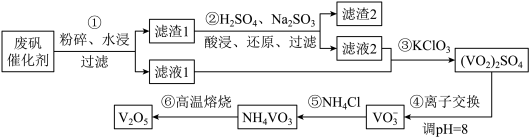
部分含钒物质在水中的溶解性见右表。回答下列问题:
(1)工业上用铝热剂法由V2O5冶炼金属钒的化学方程式为___________ 。
(2)滤渣1中含矾的物质被Na2SO3还原的离子方程式为________________________ ;
请配平滤液2中VOSO4被KClO3氧化的化学方程式:__ VOSO4+ KClO3+____ ==3(VO2)2SO4+KCl+ 3H2SO4。
(3)步骤⑤沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据右图判断沉矾最佳控制氯化铵系数和温度分别为____ 、____ ;从平衡移动角度解释沉矾过程中控制n(NH4+):n(VO3-)>1:1,原因是_______________________________ ,以保证VO3-沉淀完全。

(4)步骤⑥反应的化学方程式为_________________________________ 。
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:
VO2++V2++2H+ VO2++H2O+V3+,电池充电时阳极的电极反应式为
VO2++H2O+V3+,电池充电时阳极的电极反应式为_______ ;
若用放电的电流强度I=2.0A,电池工作10分钟,电解精炼铜得到铜mg,则电流利用效率为____ (写出表达式,不必计算出结果。已知:电量Q=It,t为时间秒;电解时Q="znF" ,z为每摩尔物质得失电子数、n为物质的量,法拉第常数F=96500C/mol, )。
)。

部分含钒物质在水中的溶解性见右表。回答下列问题:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
(2)滤渣1中含矾的物质被Na2SO3还原的离子方程式为
请配平滤液2中VOSO4被KClO3氧化的化学方程式:
(3)步骤⑤沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据右图判断沉矾最佳控制氯化铵系数和温度分别为

(4)步骤⑥反应的化学方程式为
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为:
VO2++V2++2H+
若用放电的电流强度I=2.0A,电池工作10分钟,电解精炼铜得到铜mg,则电流利用效率为
钒电池,又名全钒氧化还原液流电池,是一种酸性蓄电池,利用钒离子在不同氧化态下的不同化学势能保存能量。具有充放电效率高、容量可以随着储液罐的增加而提高,电解液可以循环利用等优点,已被多国示范运行。工作原理示意图如图所示:

已知:①VO 黄色,VO2+蓝色,V3+绿色,V2+紫色;
黄色,VO2+蓝色,V3+绿色,V2+紫色;
②NH4VO3在水溶液中是难溶物,高温分解得到一种氧化物和NH3;
③含+5价钒的微粒在溶液中主要存在形式与pH关系如下表:
回答下面问题:
(1)该电池放电时,a极得到电子发生还原反应,则a极电极反应式为___________ ,b极附近溶液颜色变化为___________ ;
(2)表格中V3O 的n=
的n=___________ ,pH在8-12时,存在V2O 和V3O
和V3O 的可逆反应,离子方程式为
的可逆反应,离子方程式为___________ ;
(3)钒电池失效后,一种回收钒的工艺流程如下:

①氧化的目的是将其它价态的钒氧化到+5价,“调pH ”的目的是___________ ,系列操作指的是___________ ,沉钒的离子方程式为____________
②钒回收率测定:将总含有钒(V)50.0mol的电池废液经过上述工艺后,充分加热NH4VO3并测得剩余固体质量为3640.0g,则钒回收率为___________ (钒回收率=实际回收得到的V的物质的量/电池废液V的总物质的量×100%)。

已知:①VO
②NH4VO3在水溶液中是难溶物,高温分解得到一种氧化物和NH3;
③含+5价钒的微粒在溶液中主要存在形式与pH关系如下表:
| pH | <2 | 3~8 | 8~12 | >12 |
| 存在形式 | VO | V3O | V2O | VO |
(1)该电池放电时,a极得到电子发生还原反应,则a极电极反应式为
(2)表格中V3O
(3)钒电池失效后,一种回收钒的工艺流程如下:

①氧化的目的是将其它价态的钒氧化到+5价,“调pH ”的目的是
②钒回收率测定:将总含有钒(V)50.0mol的电池废液经过上述工艺后,充分加热NH4VO3并测得剩余固体质量为3640.0g,则钒回收率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网