解答题-结构与性质 较难0.4 引用2 组卷343
Al、Fe、Cu 是重要的材料元素,在生产生活中有着广泛的应用。回答下列问题:
【小题1】(1)基态Fe2+的核外电子排布式为[Ar]______ ,有__ 个未成对电子。
【小题2】(2)氯化铝熔点为194℃,而氧化铝熔点为2050℃,二者熔点相差很大的原因是_____ 。
【小题3】(3)已知Al 的第一电离能为578kJ/mol、第二电离能为1817 kJ/mol、第三电离能为2745 kJ/mol、第四电离能为11575 kJ/mol。请解释其第二电离能增幅较大的原因________ 。
【小题4】(4)甲醇重整制氢反应中,铜基催化剂如CuO/SiO2具有重整温度低、催化选择性高的优点。Cu、Si、O元素电负性由大到小的顺序是____ ;SiO2中Si原子采取____ 杂化。
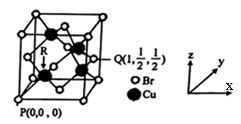
【小题5】(5)一种铜的溴化物晶胞结构如图所示:该晶胞中铜的配位数是___ ,与溴紧邻的溴原子数目是________ ,由图中P点和Q点的原子坐标参数可确定R点的原子坐标参数为________ ;已知晶胞参数为apm,其密度为_______ g/cm3 (列出计算式即可)。
【小题1】(1)基态Fe2+的核外电子排布式为[Ar]
【小题2】(2)氯化铝熔点为194℃,而氧化铝熔点为2050℃,二者熔点相差很大的原因是
【小题3】(3)已知Al 的第一电离能为578kJ/mol、第二电离能为1817 kJ/mol、第三电离能为2745 kJ/mol、第四电离能为11575 kJ/mol。请解释其第二电离能增幅较大的原因
【小题4】(4)甲醇重整制氢反应中,铜基催化剂如CuO/SiO2具有重整温度低、催化选择性高的优点。Cu、Si、O元素电负性由大到小的顺序是
【小题5】(5)一种铜的溴化物晶胞结构如图所示:该晶胞中铜的配位数是
2018·安徽马鞍山·二模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
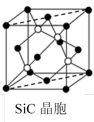
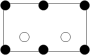
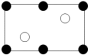
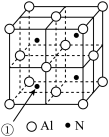

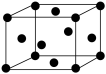 ,距离一个顶点铁原子最近的铁原子有
,距离一个顶点铁原子最近的铁原子有

