填空题 适中0.65 引用1 组卷88
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出14种元素的X的数值:
试结合元素周期律知识完成下列问题(放射性元素除外):
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。判断下列物质是离子化合物还是共价化合物?
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是______________ ; ②属于共价化合物的是______________ .
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系______________________________ ;简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系_____________________________________________ 。
(3)请你预测Br与I元素的X数值的大小关系______________________________ 。
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于_____ 原子(元素符号)。
(5)上表中元素形成的AB型化合物中,离子性最强的是_____________________
(6)请你预测周期表中X的数值最小的元素的位置________ 周期,______ 族
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | N |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 | 3.0 |
试结合元素周期律知识完成下列问题(放射性元素除外):
(1)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。判断下列物质是离子化合物还是共价化合物?
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系
(3)请你预测Br与I元素的X数值的大小关系
(4)某有机化合物分子中含有S—N键,你认为该共用电子对偏向于
(5)上表中元素形成的AB型化合物中,离子性最强的是
(6)请你预测周期表中X的数值最小的元素的位置
17-18高二下·宁夏·阶段练习
类题推荐
已知元素的电负性和原子半径一样,也是元素的基本性质。下表给出14种元素的电负性:
试结合元素周期律相关知识完成下列问题。
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是__________ (从电负性与结构的关系考虑)。
(2)请预测Br与I元素电负性的大小关系:_________ 。
(3)经验规律告诉我们:当成键的两原子相应元素的电负性差值大于1.7时,一般为离子键,而小于1.7时,一般为共价键。试推断 中化学键的类型是
中化学键的类型是 ___________ 。
(4)预测元素周期表中电负性最小的元素是_____ (放射性元素除外)。
| 元素 | AL | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
试结合元素周期律相关知识完成下列问题。
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是
(2)请预测Br与I元素电负性的大小关系:
(3)经验规律告诉我们:当成键的两原子相应元素的电负性差值大于1.7时,一般为离子键,而小于1.7时,一般为共价键。试推断
(4)预测元素周期表中电负性最小的元素是
Ⅰ.已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
试结合元素周期律知识完成下列问题:
(1)请预测K与Rb元素的X数值的大小关系:K______ Rb (填“>”、“=”或“<”)。
(2)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键,试推断AlBr3中的化学键类型是____ 。
(3)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于____ 原子(填元素符号).
(4)简述第二周期元素(除稀有气体外)的X的数值大小与原子半径之间的关系:________ 。
Ⅱ.(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
①第一步反应是____ 反应(选填“放热”或“吸热”),判断依据_____ 。
②1 molNH4+(aq)全部氧化成NO3- (aq)的热化学方程式_______ 。
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:
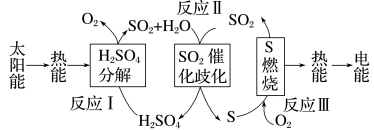
反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ/mol
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=−297 kJ/mol
反应Ⅱ的热化学方程式:_______________ 。
(3)一定条件下,不同量的CO2与不同量的NaOH充分反应放出的热量如下表所示:
写出该条件下,CO2与NaOH反应生成NaHCO3的热化学方__________________ 。
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
(1)请预测K与Rb元素的X数值的大小关系:K
(2)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键,试推断AlBr3中的化学键类型是
(3)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于
(4)简述第二周期元素(除稀有气体外)的X的数值大小与原子半径之间的关系:
Ⅱ.(1)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
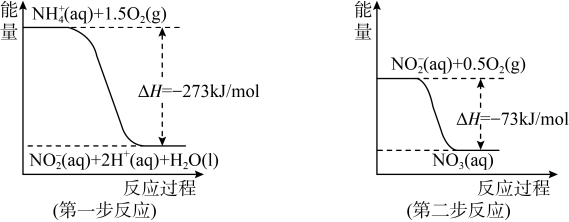
①第一步反应是
②1 molNH4+(aq)全部氧化成NO3- (aq)的热化学方程式
(2)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储,过程如下:

反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ/mol
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=−297 kJ/mol
反应Ⅱ的热化学方程式:
(3)一定条件下,不同量的CO2与不同量的NaOH充分反应放出的热量如下表所示:
| CO2的量 | NaOH的量 | 放出的热量 |
| 22.0 g | 750 mL 1.0 mol/L | x kJ |
| 1.0 mol | 2.0 L 1.0 mol/L | y kJ |
电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:答下列有关问题:
(1)预测周期表中电负性最大的元素应为____________ ;估计钙元素的电负性的取值范围:___________ < X <___________ 。
(2)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是___________ ;简述元素电负性X的大小与元素金属性、非金属性之间的关系________________ 。
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为________ ,其理由是____________________________________ 。
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)预测周期表中电负性最大的元素应为
(2)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


