解答题-实验探究题 适中0.65 引用1 组卷481
环己酮实验室合成的反应如下:
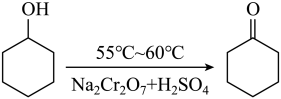
环己醇和环己酮的部分物理性质见下表:
现以20mL环己醇与足量Na2Cr2O7和硫酸的混合液充分反应,制得主要含环己酮和水的粗产品,然后进行分离提纯。其主要步骤有(未排序) :
a.蒸馏、除去乙醚后,收集151℃~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧) 萃取,萃取液并入有机层
c.往液体中加入NaCl固体至饱和,静置,分液
d.过滤
e.加入无水MgSO4固体,除去有机物中少量水
回答下列问题:
(1)上述分提纯步骤的正确顺序是_______ 。
(2)b中水层用乙醚萃取的目的是_______ 。
(3)以下关于萃取分液操作的叙述中,不正确的是_______
(4)在上述操作c中,加入NaCl固体的作用是_______ 。蒸馏除乙醚的过程中采用的加热方式为_______ 。
(5)蒸馏操作时,一段时间后发现未加沸石,应采取的正确方法是_______ 。
(6)利用红外光谱可以分析出环己酮的官能团为_______ 。
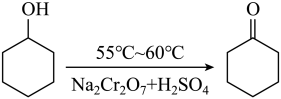
环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g·cm-3、20℃) | 溶解性 |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
a.蒸馏、除去乙醚后,收集151℃~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧) 萃取,萃取液并入有机层
c.往液体中加入NaCl固体至饱和,静置,分液
d.过滤
e.加入无水MgSO4固体,除去有机物中少量水
回答下列问题:
(1)上述分提纯步骤的正确顺序是
(2)b中水层用乙醚萃取的目的是
(3)以下关于萃取分液操作的叙述中,不正确的是_______
A.水溶液中加入乙醚,转移至分液漏斗,塞上玻璃塞,如图用力振荡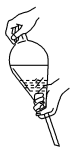 |
| B.振荡几次后需打开分液漏斗上口的玻璃塞放气 |
| C.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体 |
| D.经几次振荡并放气后,手持分漏斗静置液体分层 |
(5)蒸馏操作时,一段时间后发现未加沸石,应采取的正确方法是
(6)利用红外光谱可以分析出环己酮的官能团为
2018·河南·一模
类题推荐
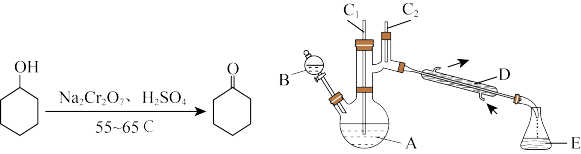
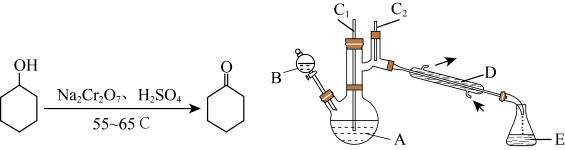
实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略)如下:
有关物质的物理性质见下表。
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,55~60℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为___________________ 。
(2)实验时加入沸石的作用_______________ ,若加热后发现未加沸石,应采取的正确操作是_______________ 。
(3)蒸馏不能分离环己酮和水的原因是_______________ 。
(4)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是_______________ ;
②b中水层用乙醚萃取的目的是_______________ ;
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、漏斗外,还需要的玻璃仪器有_______________ ,操作d中,加入NaCl固体的作用是_______________ 。
(5)恢复至室温时,分离得到纯产品5.7g,则环已酮的产率_______________ (计算结果精确到0.1%)。

有关物质的物理性质见下表。
| 物质 | 沸点(℃) | 密度(g·cm−3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中,55~60℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为
(2)实验时加入沸石的作用
(3)蒸馏不能分离环己酮和水的原因是
(4)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是
②b中水层用乙醚萃取的目的是
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、漏斗外,还需要的玻璃仪器有
(5)恢复至室温时,分离得到纯产品5.7g,则环已酮的产率
环己酮是重要的化工原料,是制造尼龙的主要中间体,也是重要的工业溶剂,实验室利用如下反应原理和实验装置(部分夹持装置略去)制备环己酮:

有关物质的物理性质见下表。
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中在55~65℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称是___________ ;该制备过程采用的加热方式为___________ 。
(2)A中发生反应的离子方程式为___________ 。(已知: 会生成
会生成 )
)
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是___________ ;
②d中往液体中加入NaCl固体的目的是___________ ;
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有___________ 。
④a操作中加热后发现忘记加入碎瓷片,应___________ 。

有关物质的物理性质见下表。
| 物质 | 沸点/℃ | 溶解性 | |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 | - |
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中在55~65℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称是
(2)A中发生反应的离子方程式为
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是
②d中往液体中加入NaCl固体的目的是
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有
④a操作中加热后发现忘记加入碎瓷片,应
环己酮是重要的化工原料,是制造尼龙的主要中间体,也是重要的工业溶剂,实验室利用如下反应原理和实验装置(部分夹持装置略去)制备环己酮:
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中在55~65℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称是___________ ,该制备过程采用的加热方式为___________ 。
(2)A中发生反应的离子方程式为___________ 。(已知: 会生成Cr3+)
会生成Cr3+)
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是___________ 。
②d中往液体中加入NaCl固体的目的是___________ 。
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有___________ 。
④a操作中加入碎瓷片的作用是___________ 。
| 物质 | 沸点/℃ | 密度( | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
| 环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 1.0 | - |
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10mL环己醇的A中在55~65℃进行反应。反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称是
(2)A中发生反应的离子方程式为
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是
②d中往液体中加入NaCl固体的目的是
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有
④a操作中加入碎瓷片的作用是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


