解答题-原理综合题 较难0.4 引用1 组卷167
党的十九大报告指出:要持续实施大气污染防治行动,打赢蓝天保卫战。当前空气质量检测的主要项目除了PM2.5外,还有CO、SO2、氮氧化物(NO和NO2)、O3等气体。
(1)汽车尾气中含有NO 和CO气体,可利用催化剂对CO、NO进行催化转化反应:
2CO(g) +2NO(g)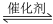 N2(g) +2CO2(g) △H
N2(g) +2CO2(g) △H
① 已知下列热化学方程式:
N2(g) +O2(g) =2NO(g) △H1 = + 180.5kJ/mol
2C(s) +O2(g) =2CO(g) △H2=-2210kJ/mol
C(s)+O2(g)=CO2(g) △H3=-393.5kJ/mol
则 △H=_________ 。
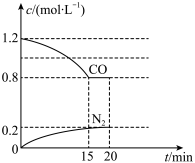
②在一定温度下,将2.0molNO、2.4molCO气体通入到固定容积为2 L的密闭容器中,反应过程中部分物质的浓度变化如下图所示。在0~15min,以N2 表示的该反应的平均速度v(N2)=________ 。若保持反应体系温度不变,20min时再容器中充入NO、N2 各0.4mol,化学平衡将_____ 移动 (填“向左”“向右”或“不”)。
(2)在相同温度下,两个体积均为1L 的恒容密闭容器中,发生CO、NO催化转化反应,有关物质的量如下表:
①容器I中平衡后气体的压强为开始时的0.875倍,则a=________ 。
②容器II平衡时的气体压强为p,用平衡分压代替平衡浓度表示的平衡常数K 为________ 。
(3)汽车使用乙醇汽油并不能破少NOx的排放。某研究小组在实验室以耐高温试剂Ag-ZSW-5对CO、NO 催化转化进行研究。测得NO 转化为N 2的转化率随温度CO 混存量的变化情况如图所示。
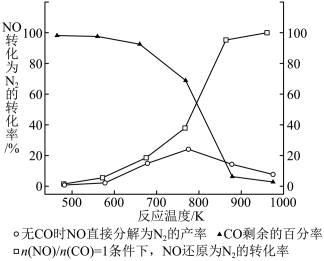
①在n(NO)/n(CO) =1条件下,最佳温度应控制在_______ 左右。
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为________ 。
③加入CO后NO转化为N2 的转化率增大的原因是_______ (用平衡移动的原理解释)。
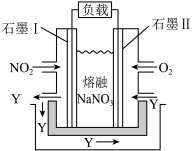
(4)以NO2、O2、熔融NaNO3 组成的燃料电池装置如右图所示,在使用过程中石墨I电极反应生成一种氧化物Y,则该电极反应式为_______ 。
(1)汽车尾气中含有NO 和CO气体,可利用催化剂对CO、NO进行催化转化反应:
2CO(g) +2NO(g)
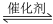 N2(g) +2CO2(g) △H
N2(g) +2CO2(g) △H① 已知下列热化学方程式:
N2(g) +O2(g) =2NO(g) △H1 = + 180.5kJ/mol
2C(s) +O2(g) =2CO(g) △H2=-2210kJ/mol
C(s)+O2(g)=CO2(g) △H3=-393.5kJ/mol
则 △H=
②在一定温度下,将2.0molNO、2.4molCO气体通入到固定容积为2 L的密闭容器中,反应过程中部分物质的浓度变化如下图所示。在0~15min,以N2 表示的该反应的平均速度v(N2)=

(2)在相同温度下,两个体积均为1L 的恒容密闭容器中,发生CO、NO催化转化反应,有关物质的量如下表:
| 容器编号 | 起始物质的量/mol | 平衡物质的量/mol | |||
| NO | CO | N2 | CO2 | CO2 | |
| I | 0.2 | 0.2 | 0 | 0 | a |
| II | 0.3 | 0.3 | b | 0.1 | 0.2 |
②容器II平衡时的气体压强为p,用平衡分压代替平衡浓度表示的平衡常数K 为
(3)汽车使用乙醇汽油并不能破少NOx的排放。某研究小组在实验室以耐高温试剂Ag-ZSW-5对CO、NO 催化转化进行研究。测得NO 转化为N 2的转化率随温度CO 混存量的变化情况如图所示。

①在n(NO)/n(CO) =1条件下,最佳温度应控制在
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为
③加入CO后NO转化为N2 的转化率增大的原因是
(4)以NO2、O2、熔融NaNO3 组成的燃料电池装置如右图所示,在使用过程中石墨I电极反应生成一种氧化物Y,则该电极反应式为

2018·新疆乌鲁木齐·二模
类题推荐
对机动车尾气中的N元素、C 元素进行处理,可以保护环境,减少污染。
(1)汽缸中生成 NO 的反应为:N2(g)+O2(g) 2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
反应Ⅰ:NO(g)+CO(g)+Rh(s) RhN(s)+CO2(g) △H=-8 kcal·mol-1
RhN(s)+CO2(g) △H=-8 kcal·mol-1
反应Ⅱ:RhN(s)+NO(g) Rh(s)+N2O △H =-76.4 kcal·mol -1
Rh(s)+N2O △H =-76.4 kcal·mol -1
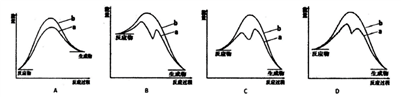
则由NO生成2 mol N2O的△H =_________ kcal·mol-1。若Ⅰ比Ⅱ的反应速率大,下列能正确表示反应2NO(g)+CO(g) N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应过程的能量变化图的是
N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应过程的能量变化图的是________________ 。
(2)相同温度下,两个体积均为1L的恒容密闭容器中,发生反应:
2NO(g)+2CO (g)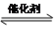 N2(g)+2CO2(g),有关物质的量如下表:
N2(g)+2CO2(g),有关物质的量如下表:
①容器Ⅰ中平衡后气体的压强为开始时的0.875 倍,则a =_________________ 。
②容器Ⅱ平衡时的气体压强为p,用平衡分压代替平衡浓度表示的平衡常数K为_________ 。(3) 汽车使用乙醇汽油并不能减少NOx的排放,某研究小组在实验室以耐高温试剂Ag-ZSW-5催化,测得NO转化为N2的转化率随温度变化情况如下图所示。
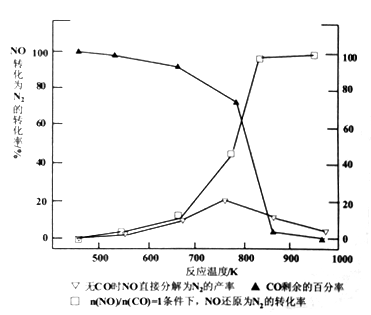
①在n(NO)/n(CO)=1条件下,最佳温度应控制在_____ 左右。
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为_______________ 。
③用平衡移动原理解释为什么加入CO后NO转化为N2的转化率增大?__________________ 。
(1)汽缸中生成 NO 的反应为:N2(g)+O2(g)
 2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):反应Ⅰ:NO(g)+CO(g)+Rh(s)
 RhN(s)+CO2(g) △H=-8 kcal·mol-1
RhN(s)+CO2(g) △H=-8 kcal·mol-1反应Ⅱ:RhN(s)+NO(g)
 Rh(s)+N2O △H =-76.4 kcal·mol -1
Rh(s)+N2O △H =-76.4 kcal·mol -1则由NO生成2 mol N2O的△H =
 N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应过程的能量变化图的是
N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应过程的能量变化图的是
(2)相同温度下,两个体积均为1L的恒容密闭容器中,发生反应:
2NO(g)+2CO (g)
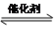 N2(g)+2CO2(g),有关物质的量如下表:
N2(g)+2CO2(g),有关物质的量如下表:| 容器 编号 | 起始物质的量/mol | 平衡物质的量/mol | |||
| NO | CO | N2 | CO2 | CO2 | |
| Ⅰ | 0.2 | 0.2 | 0 | 0 | a |
| Ⅱ | 0.3 | 0.3 | b | 0.1 | 0.2 |
①容器Ⅰ中平衡后气体的压强为开始时的0.875 倍,则a =
②容器Ⅱ平衡时的气体压强为p,用平衡分压代替平衡浓度表示的平衡常数K为

①在n(NO)/n(CO)=1条件下,最佳温度应控制在
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为
③用平衡移动原理解释为什么加入CO后NO转化为N2的转化率增大?
氮的氧化物是大气污染物,可以通过以下方法处理:
I.催化还原法:在汽车排气管上安装一个催化转化器,发生反应:
2NO(g) + 2CO(g) N2(g) + 2CO2(g) △H1
N2(g) + 2CO2(g) △H1
(1)已知:①N2(g) +O2(g) 2NO(g) △H2=+180kJ/mol
2NO(g) △H2=+180kJ/mol
②CO与O2 反应相关的化学键键能数据如下:
则△H1=__________ 。
(2)在一定温度下,向容积为1L的密闭容器中充入2 molNO、1molCO,10min时反应2NO(g)+2CO(g) N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图1所示:
N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图1所示:

①该反应的平衡常数K=______ (结果保留3位有效数字);前10min内用氮气表示的平均反应速率为______ 。
②若保持其他条件不变,15min时再向该容器中充入少量N2,则此时反应的v正______ v逆(填“>”、“=”或“<”),原因是____________ 。
③若保持其他条件不变,15min时压缩容器的容积至0.5L,20min时反应重新达到平衡,则此时NO的浓度对应的点应是图1中的______ (填字母)。
④某科研小组研究发现以Ag-ZSM-5为催化剂,NO转化为N2的转化率随温度变化情况如图2 所示。若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因是______ 。
II.利用电化学原理,将NO2、O2 和熔融KNO3制成燃料电池,其原理如图3。
(3)该电池在工作过程中NO2转变成绿色硝化剂Y,Y 是一种氧化物,可循环使用,石墨I附近发生的电极反应式为______ 。相同条件下,消耗的O2 和NO2 的体积比为______ 。
I.催化还原法:在汽车排气管上安装一个催化转化器,发生反应:
2NO(g) + 2CO(g)
 N2(g) + 2CO2(g) △H1
N2(g) + 2CO2(g) △H1(1)已知:①N2(g) +O2(g)
 2NO(g) △H2=+180kJ/mol
2NO(g) △H2=+180kJ/mol②CO与O2 反应相关的化学键键能数据如下:
| 化学键 | O=O | C=O | C≡O |
| 键能/(kJ/mol) | 497 | 803 | 1072 |
则△H1=
(2)在一定温度下,向容积为1L的密闭容器中充入2 molNO、1molCO,10min时反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图1所示:
N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图1所示:
①该反应的平衡常数K=
②若保持其他条件不变,15min时再向该容器中充入少量N2,则此时反应的v正
③若保持其他条件不变,15min时压缩容器的容积至0.5L,20min时反应重新达到平衡,则此时NO的浓度对应的点应是图1中的
④某科研小组研究发现以Ag-ZSM-5为催化剂,NO转化为N2的转化率随温度变化情况如图2 所示。若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因是
II.利用电化学原理,将NO2、O2 和熔融KNO3制成燃料电池,其原理如图3。
(3)该电池在工作过程中NO2转变成绿色硝化剂Y,Y 是一种氧化物,可循环使用,石墨I附近发生的电极反应式为
对机动车尾气中的N元素、C 元素进行处理,可以保护环境,减少污染。
(1)汽缸中生成 NO 的反应为:N2(g)+O2(g) 2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
反应Ⅰ:NO(g)+CO(g)+Rh(s) RhN(s)+CO2(g) △H=-8kcal·mol-1
RhN(s)+CO2(g) △H=-8kcal·mol-1
反应Ⅱ:RhN(s)+NO(g) Rh(s)+N2O(g) △H =-76.4kcal·mol-1
Rh(s)+N2O(g) △H =-76.4kcal·mol-1
则由NO生成1mol N2O的△H =____ kcal·mol-1。若Ⅰ比Ⅱ的反应速率大,下列能正确表示反应2NO(g)+CO(g) N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应进程的能量变化图的是
N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应进程的能量变化图的是_____

⑵在体积为1L的恒温密闭容器中,发生反应:
2NO(g)+2CO (g)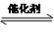 N2(g)+2CO2(g),有关物质的量如下表:
N2(g)+2CO2(g),有关物质的量如下表:
①上述反应的化学平衡常数表达式K=__________
②若达到平衡后气体的压强为开始时的0.875倍,则a =______
⑶汽车使用乙醇汽油并不能减少NOx的排放,某研究小组在实验室以耐高温试剂Ag-ZSW-5催化,测得NO转化为N2的转化率随温度变化情况如下图所示。

①在n(NO)/n(CO)=1条件下,最佳温度应控制在_____ 左右。
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为___
③用平衡移动原理解释为什么加入CO后NO转化为N2的转化率增大?______
(1)汽缸中生成 NO 的反应为:N2(g)+O2(g)
 2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):
2NO(g) △H>0,NOx在铑(Rh)的催化下最终转化为无毒的产物,其中NO与CO的反应过程中经历如下两步(已知:1kcal=4.18kJ):反应Ⅰ:NO(g)+CO(g)+Rh(s)
 RhN(s)+CO2(g) △H=-8kcal·mol-1
RhN(s)+CO2(g) △H=-8kcal·mol-1反应Ⅱ:RhN(s)+NO(g)
 Rh(s)+N2O(g) △H =-76.4kcal·mol-1
Rh(s)+N2O(g) △H =-76.4kcal·mol-1则由NO生成1mol N2O的△H =
 N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应进程的能量变化图的是
N2O(g)+CO2(g) △H在有催化剂(a)和无催化剂(b)时反应进程的能量变化图的是
⑵在体积为1L的恒温密闭容器中,发生反应:
2NO(g)+2CO (g)
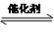 N2(g)+2CO2(g),有关物质的量如下表:
N2(g)+2CO2(g),有关物质的量如下表:| 起始物质的量/mol | 平衡物质的量/mol | |||
| NO | CO | N2 | CO2 | CO2 |
| 0.2 | 0.2 | 0 | 0 | a |
①上述反应的化学平衡常数表达式K=
②若达到平衡后气体的压强为开始时的0.875倍,则a =
⑶汽车使用乙醇汽油并不能减少NOx的排放,某研究小组在实验室以耐高温试剂Ag-ZSW-5催化,测得NO转化为N2的转化率随温度变化情况如下图所示。

①在n(NO)/n(CO)=1条件下,最佳温度应控制在
②若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因为
③用平衡移动原理解释为什么加入CO后NO转化为N2的转化率增大?
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


