解答题-实验探究题 适中0.65 引用2 组卷234
硼是第IIIA族元素,单质硼在加热条件下能与多种非金属反应。某同学欲利用氯气 和单质硼 反应制备三氯化硼。已知BC13的沸点为12.5 ℃ ,熔点为-107.3 ℃,遇水剧烈反应,生成硼酸和盐酸。该同学选用下图所示的部分装置(可以重复选用)进行实验,请回答下列问题:
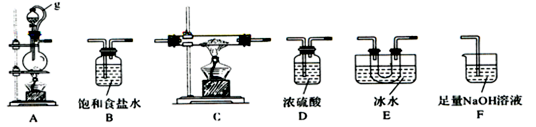
(1)A中反应的离子方程式为__________________ 。
(2)图中g管的作用是______________________________________ 。
(3)装置的连接顺序依次为A→ → → →E→D→F;____________ 在E、F装置间连接D装置的作用是____________________________________________________________ 。
(4)停止实验时,正确的实验操作是______________________________________________________________________________________________________________ 。
(5)若硼酸(H3BO3)为一元弱酸,则其钠盐NaH2BO3为_____ (填“正盐”或“酸式盐”或“碱式盐”)。
(6)实验完成后,某同学向F中(溶液含有0.05mol/LNaClO、 0.05mol/LNaCl、0.1mol/LNaOH)滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因,请在表中空格处填上数据,完成实验方案。
则x=_______ ,结论:________________________________________________ 。

(1)A中反应的离子方程式为
(2)图中g管的作用是
(3)装置的连接顺序依次为A→ → → →E→D→F;
(4)停止实验时,正确的实验操作是
(5)若硼酸(H3BO3)为一元弱酸,则其钠盐NaH2BO3为
(6)实验完成后,某同学向F中(溶液含有0.05mol/LNaClO、 0.05mol/LNaCl、0.1mol/LNaOH)滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因,请在表中空格处填上数据,完成实验方案。
| 实验序号 | 0.1mol/LNaClO溶液/mL | 0.1mol/LNaCl溶液/mL | 0.2mol/LNaOH溶液/mL | H2O /mL | 品红 溶液 | 现象 |
| ① | 5.0 | 0 | 0 | x | 4滴 | 较快褪色 |
| ② | 0 | 5.0 | 5.0 | 0 | 4滴 | 不褪色 |
| ③ | 5.0 | 0 | 5.0 | 0 | 4滴 | 缓慢褪色 |
2018·广东汕头·一模
类题推荐
三氯化硼(BC13,沸点为12.5℃,熔点为-107.3℃)可用作有机合成催化剂,某化学兴趣小组利用氯气和单质硼反应制备三氯化硼。已知三氯化硼遇水剧烈反应,生成硼酸(H3BO3为一元弱酸)和盐酸。该兴趣小组利用如图所示的部分装置(可重复选用)进行实验。
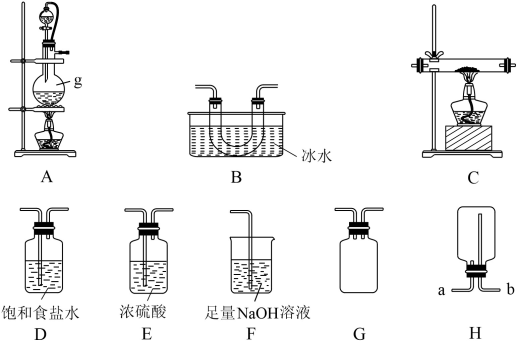
(1)仪器g的名称是_____ ,若用装置H收集氯气,气体应从_____ (填“a”或“b”)进入。
(2)装置的连接顺序依次为A→____ →____ →____ →____ →____ →____ →F,装置G的作用是:______ 。
(3)NaH2BO3的电离方程式为_______ 。
(4)实验完成后,某同学向装置F中(溶液含有0.1mol∙L-1NaClO、0.1mol∙L-1NaCl、0.2mol∙L-1NaOH)滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因。
则x=______ ,由实验得出的结论是_________________ 。
(5)NaOH溶液常用于酸碱中和滴定。在规格为50.00mL的碱式滴定管中,若NaOH溶液起始读数为20.00mL,此时滴定管中NaOH溶液的实际体积为_______ 。
(6)H3BO3可由硼砂(Na2B4O7∙10H2O)与盐酸在加热的条件下反应制得,该反应的化学方程_______ 。

(1)仪器g的名称是
(2)装置的连接顺序依次为A→
(3)NaH2BO3的电离方程式为
(4)实验完成后,某同学向装置F中(溶液含有0.1mol∙L-1NaClO、0.1mol∙L-1NaCl、0.2mol∙L-1NaOH)滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因。
| 实验序号 | 0.2mol∙L-1 NaClO/mL | 0.2mol∙L-1 NaCl/mL | 0.4mol∙L-1 NaOH/mL | H2O/mL | 品红溶液 | 现象 |
| Ⅰ | 0.0 | 15.0 | 15.0 | 0.0 | 4滴 | 不褪色 |
| Ⅱ | 15.0 | 0.0 | 15.0 | 0.0 | 4滴 | 缓慢褪色 |
| Ⅲ | 15.0 | 0.0 | 0.0 | x | 4滴 | 较快褪色 |
(5)NaOH溶液常用于酸碱中和滴定。在规格为50.00mL的碱式滴定管中,若NaOH溶液起始读数为20.00mL,此时滴定管中NaOH溶液的实际体积为
(6)H3BO3可由硼砂(Na2B4O7∙10H2O)与盐酸在加热的条件下反应制得,该反应的化学方程
三氯化硼(BC13,沸点为12.5℃,熔点为-107.3℃)可用作有机合成催化剂,某化学兴趣小组利用氯气和单质硼反应制备三氯化硼。已知三氯化硼遇水剧烈反应,生成硼酸(H3BO3为一元弱酸)和盐酸。该兴趣小组利用如图所示的部分装置(可重复选用)进行实验。
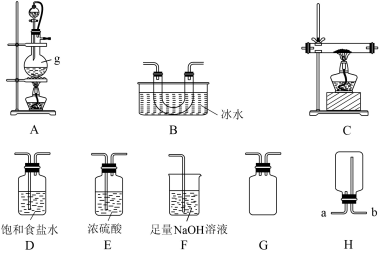
(1)仪器g的名称是___________ ,若用装置H收集氯气,气体应从___________ (填“a”或“b”)进入。
(2)装置的连接顺序依次为______ ,A→______→______→______→_____→______→_____→F,装置G的作用是:_______ 。
(3)NaH2BO3的电离方程式为___________ 。
(4)实验完成后,某同学向装置F中(溶液含有0.1mol∙L-1NaClO、0.1mol∙L-1NaCl、0.2mol∙L-1NaOH)滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因。
则x=___________ ,由实验得出的结论是___________ 。

(1)仪器g的名称是
(2)装置的连接顺序依次为
(3)NaH2BO3的电离方程式为
(4)实验完成后,某同学向装置F中(溶液含有0.1mol∙L-1NaClO、0.1mol∙L-1NaCl、0.2mol∙L-1NaOH)滴加品红溶液,发现溶液褪色。现设计实验探究溶液褪色的原因。
| 实验序号 | 0.2mol∙L-1NaClO/mL | 0.2mol∙L-1NaCl/mL | 0.4mol∙L-1NaOH/mL | H2O/mL | 品红溶液 | 现象 |
| I | 0.0 | 15.0 | 15.0 | 0.0 | 4滴 | 不褪色 |
| II | 15.0 | 0.0 | 15.0 | 0.0 | 4滴 | 缓慢褪色 |
| III | 15.0 | 0.0 | 0.0 | x | 4滴 | 较快褪色 |
为了更深刻地认识卤素的性质,某化学小组对卤素及其化合物的制备和性质进行如下探究实验,根据实验回答问题。
[实验一]氯气的制备
(1)该小组拟用图甲实验装置来制备纯净、干燥的氯气,并完成与金属铁的反应(夹持仪器略去)。每个虚线框表示一个单元装置,请用文字描述将下列装置的错误之处改正:___ 。

[实验二]探究氯化亚铁与氧气反应的产物
已知氯化亚铁的熔点为674℃,沸点为1023℃;三氯化铁在100℃左右时升华,极易水解。在500℃条件下氯化亚铁与氧气可能发生下列反应:12FeCl2+3O2 2Fe2O3+8FeCl3、4FeCl2+3O2
2Fe2O3+8FeCl3、4FeCl2+3O2 2Fe2O3 +4Cl2,该化学小组选用图乙部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。
2Fe2O3 +4Cl2,该化学小组选用图乙部分装置(装置可以重复选用)进行氯化亚铁与氧气反应产物的探究。

(2)实验装置的合理连接顺序为A→___ →E。
(3)简述将装置F中的固体配成溶液的操作方法:___ 。
[实验三]卤素化合物之间反应的实验条件控制探究
(4)在不同实验条件下KClO3可将KI氧化为I2或KIO3。该小组同学设计的一组实验的数据记录如下表(实验控制在室温下进行):
①该组实验的目的是___ 。
②2号试管反应完全后,取少量试管中的溶液,滴加淀粉溶液后显蓝色,假设还原产物只有KCl,写出反应的离子方程式:___ 。
[实验一]氯气的制备
(1)该小组拟用图甲实验装置来制备纯净、干燥的氯气,并完成与金属铁的反应(夹持仪器略去)。每个虚线框表示一个单元装置,请用文字描述将下列装置的错误之处改正:

[实验二]探究氯化亚铁与氧气反应的产物
已知氯化亚铁的熔点为674℃,沸点为1023℃;三氯化铁在100℃左右时升华,极易水解。在500℃条件下氯化亚铁与氧气可能发生下列反应:12FeCl2+3O2

(2)实验装置的合理连接顺序为A→
(3)简述将装置F中的固体配成溶液的操作方法:
[实验三]卤素化合物之间反应的实验条件控制探究
(4)在不同实验条件下KClO3可将KI氧化为I2或KIO3。该小组同学设计的一组实验的数据记录如下表(实验控制在室温下进行):
| 试管标号 | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI溶液/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4溶液/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
②2号试管反应完全后,取少量试管中的溶液,滴加淀粉溶液后显蓝色,假设还原产物只有KCl,写出反应的离子方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


