解答题-结构与性质 0.65 引用2 组卷284
铜及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是_____ (填字母)。
a.电子从基态跃迁到较高的激发态 b.电子从较高的激发态跃迁到基态
c.焰色反应的光谱属于吸收光谱 d.焰色反应的光谱属于发射光谱
(2)基态Cu原子中,核外电子占据的最高能层符号是_____ ,其核外电子排布式中未成对电子数为______ 个,Cu与Ag均属于IB族,熔点:Cu____ Ag(填“>”或“<”)。
(3)[Cu(NH3)4]SO4中阴离子的立体构型是_________ ;中心原子的轨道杂化类型为__________ ,[Cu(NH3)4]SO4中Cu2+与NH3之间形成的化学键称为________________ 。
(4)用Cu作催化剂可以氧化乙醇生成乙醛,乙醛中σ键和π键的比值为___________ 。
(5)碘、铜两种元素的电负性如表:
CuI属于_______ (填“共价”或“离子”)化合物。
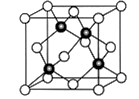
(6)Cu 与Cl 形成某种化合物的晶胞如图所示,该晶体的密度为ρg·cm-3,晶胞边长为a cm,则阿伏伽德罗常数为__________ (用含ρ、a的代数式表示)。
(1)铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是
a.电子从基态跃迁到较高的激发态 b.电子从较高的激发态跃迁到基态
c.焰色反应的光谱属于吸收光谱 d.焰色反应的光谱属于发射光谱
(2)基态Cu原子中,核外电子占据的最高能层符号是
(3)[Cu(NH3)4]SO4中阴离子的立体构型是
(4)用Cu作催化剂可以氧化乙醇生成乙醛,乙醛中σ键和π键的比值为
(5)碘、铜两种元素的电负性如表:
| 元素 | I | Cu |
| 电负性 | 2.5 | 1.9 |
(6)Cu 与Cl 形成某种化合物的晶胞如图所示,该晶体的密度为ρg·cm-3,晶胞边长为a cm,则阿伏伽德罗常数为
2018·河南濮阳·二模


