解答题-工业流程题 较难0.4 引用1 组卷306
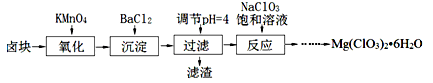
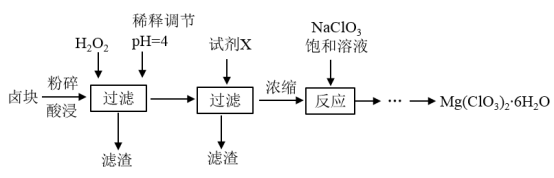
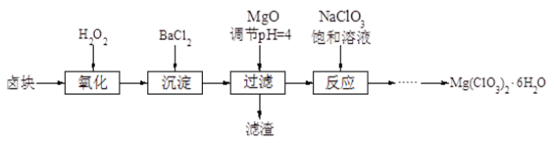
氯酸镁常用作催熟剂、除草剂等,实验室制备Mg(C1O3)2·6H2O 的流程如下:

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
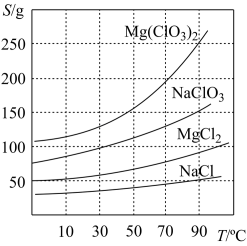
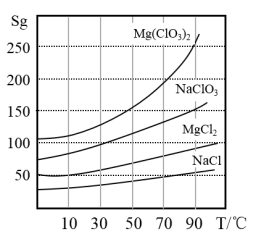
②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。
(1)过滤所需要的主要玻璃仪器有_________ 。
(2)加MgO后过滤所得滤渣的主要成分的化学式为_________ 。
(3)加入NaClO3饱和溶液后发生反应的化学方程式为__________ ,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:①________ ;______ ;洗涤;②将滤液冷却结晶;③过滤、洗涤。
(4)产品中Mg(ClO3)2·6H2O含量的测定:(已知Mg(ClO3)2·6H2O的摩尔质量为299 g/mol)
步骤1:准确称量3.50g产品配成100 mL溶液。
步骤2:取10.00mL于锥形瓶中,加入10.00mL稀硫酸和20.00mL1.000mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100mol/LK2Cr2O7 溶液滴定剩余的Fe2+至终点。反应的方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7 溶液15.00mL。
① 写出步骤2中发生反应的离子方程式__________ ;
② 产品中Mg(ClO3)2·6H2O的质量分数为_______ 。(保留到小数点后一位)

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。

(1)过滤所需要的主要玻璃仪器有
(2)加MgO后过滤所得滤渣的主要成分的化学式为
(3)加入NaClO3饱和溶液后发生反应的化学方程式为
(4)产品中Mg(ClO3)2·6H2O含量的测定:(已知Mg(ClO3)2·6H2O的摩尔质量为299 g/mol)
步骤1:准确称量3.50g产品配成100 mL溶液。
步骤2:取10.00mL于锥形瓶中,加入10.00mL稀硫酸和20.00mL1.000mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100mol/LK2Cr2O7 溶液滴定剩余的Fe2+至终点。反应的方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7 溶液15.00mL。
① 写出步骤2中发生反应的离子方程式
② 产品中Mg(ClO3)2·6H2O的质量分数为
17-18高三·四川成都·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
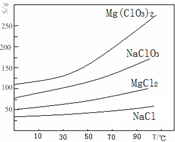
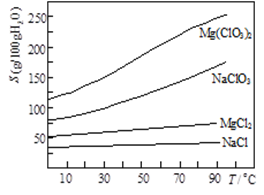
 Mg(ClO3)2+2NaCl↓,请利用该反应,结合右图,制取Mg(ClO3)2·6H2O的实验步骤依次为: ①取样,加入NaClO3饱和溶液充分反应,②蒸发结晶;③
Mg(ClO3)2+2NaCl↓,请利用该反应,结合右图,制取Mg(ClO3)2·6H2O的实验步骤依次为: ①取样,加入NaClO3饱和溶液充分反应,②蒸发结晶;③

