解答题-工业流程题 较难0.4 引用2 组卷448
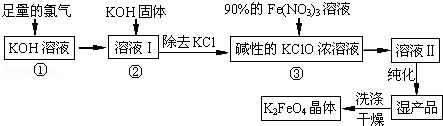
高铁酸钾(K2FeO4)是新型多功能水处理剂。其生产工艺如下:

回答下列问题:
(1)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,写出温度较高时反应的离子方程式____________ 。
(2)在溶液I中加入NaOH固体的目的是_______ (填字母)。
A.与反应液I中过量的Cl2继续反应,生成更多的NaClO
B.NaOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使NaClO3转化为NaClO
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。图1为不同的温度下,不同质量浓度的Fe(NO3)3对K2FeO4生成率的影响;图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4的生成率的影响。
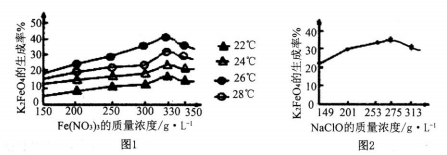
工业生产中最佳温度为_______ ,此时Fe(NO3)3与NaClO两种溶液的最佳质量浓度之比为_____ 。
(4)反应③中的离子反应方程式为_________________ ;溶液Ⅱ中加入饱和KOH得到湿产品的原因是__________________ 。
(5)高铁酸钾作为水处理剂是能与水反应其离子反应是: +l0H2O=4Fe(OH)3(胶体)十3O2↑+8OH-。则其作为水处理剂的原理是:①
+l0H2O=4Fe(OH)3(胶体)十3O2↑+8OH-。则其作为水处理剂的原理是:①_______________ ;②_______________ 。

回答下列问题:
(1)反应①应在温度较低的情况下进行,因温度较高时NaOH与Cl2反应生成NaClO3,写出温度较高时反应的离子方程式
(2)在溶液I中加入NaOH固体的目的是
A.与反应液I中过量的Cl2继续反应,生成更多的NaClO
B.NaOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供碱性的环境
D.使NaClO3转化为NaClO
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。图1为不同的温度下,不同质量浓度的Fe(NO3)3对K2FeO4生成率的影响;图2为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4的生成率的影响。

工业生产中最佳温度为
(4)反应③中的离子反应方程式为
(5)高铁酸钾作为水处理剂是能与水反应其离子反应是:
18-19高三上·安徽合肥·期末
类题推荐
高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定,是一种新型多功能水处理剂。其生产工艺如图1所示:
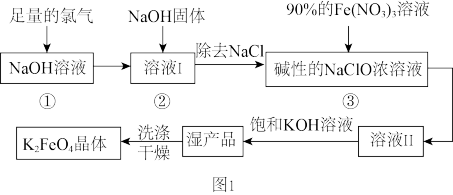
回答下列问题:
(1)反应①应在温度较低的情况下进行,因温度较高时 NaOH 与Cl2反应生成NaClO3,取某温度下反应液,测得ClO-与 的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为
的物质的量浓度之比是2∶1,则Cl2与氢氧化钠溶液反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为_______ 。
(2)在溶液I中加入 NaOH 固体的目的是_______(填字母)。
(3)反应③的离子方程式为_______ ,制备时,两溶液混合的操作为_______ 。
(4)往溶液II中加入饱和 KOH溶液得到湿产品的原因是_______ 。该工艺流程中可循环使用的物质是_______ (填化学式)。
(5)高铁酸钾还可以通过电解法制备,其原理如图2所示:
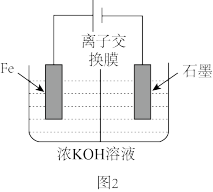
阳极的电极反应式为_______ 。该方法操作简便,成功率高,易于实验室制备。缺点是产品纯度低,其原因是_______ 。

回答下列问题:
(1)反应①应在温度较低的情况下进行,因温度较高时 NaOH 与Cl2反应生成NaClO3,取某温度下反应液,测得ClO-与
(2)在溶液I中加入 NaOH 固体的目的是_______(填字母)。
| A.使 NaClO3转化为 NaClO |
| B.为下一步反应提供碱性的环境 |
| C.NaOH 固体溶解时会放出较多的热量,有利于提高反应速率 |
| D.与溶液I中过量的Cl2继续反应,生成更多的NaClO |
(4)往溶液II中加入饱和 KOH溶液得到湿产品的原因是
(5)高铁酸钾还可以通过电解法制备,其原理如图2所示:

阳极的电极反应式为
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:

已知:
①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)该生产工艺应在_____________ (填“温度较高”或“温度较低”)情况下进行;
(2)写出工业上制取Cl2的化学方程式___________________________ ;
(3)K2 FeO4可作为新型多功能水处理剂的原因是_________________________ ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为___________ ;
(5)在“反应液I”中加KOH固体的目的是___________ :
(6)从“反应液II”中分离出K2FeO4后,会有副产品__________________ (写化学式)。
(7)该工艺每得到1.98 kg K2FeO4,理论上消耗Cl2的物质的量为__________ mol。

已知:
①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+3KClO+10KOH=2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)该生产工艺应在
(2)写出工业上制取Cl2的化学方程式
(3)K2 FeO4可作为新型多功能水处理剂的原因是
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为
(5)在“反应液I”中加KOH固体的目的是
| A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
| C.为下一步反应提供反应物 |
| D.使副产物KClO3转化为 KClO |
(6)从“反应液II”中分离出K2FeO4后,会有副产品
(7)该工艺每得到1.98 kg K2FeO4,理论上消耗Cl2的物质的量为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网