解答题-原理综合题 较难0.4 引用2 组卷413
COS 和H2S 是许多煤化工产品的原料气。已知:
Ⅰ.COS(g)+H2(g) H2S(g)+CO(g) ΔH=X kJ·mol-1;
H2S(g)+CO(g) ΔH=X kJ·mol-1;
I.CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-42 kJ·mol-1;
CO2(g)+H2(g) ΔH=-42 kJ·mol-1;
(1)断裂1mol分子中的化学键所需吸收的能量如下表所示:
则X=_____________________ 。
(2)向10 L容积不变的密闭容器中充入1mol COS(g)、1mol H2(g)和1mol H2O(g),进行上述两个反应,在某温度下达到平衡,此时CO的体积分数为4%,且测得此时COS的物质的量为0.80mol,则该温度下反应I的平衡常数为_________________ (保留两位有效数字)
(3)现有两个相同的2 L恒容绝热(与外界没有热量交换)密闭容器M、N,在M 中充入1mol CO和1molH2O,在N 中充入1molCO2和1molH2,均在700℃下开始按Ⅱ进行反应。达到平衡时,下列说法正确的是_________ 。
A.两容器中CO 的物质的量M>N
B.两容器中正反应速率M
C.容器M 中CO的转化率与容器N 中CO2的转化率之和小于1
D.两容器中反应的平衡常数M>N
(4)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
煤的气化过程中产生的H2S 可用足量的Na2CO3溶液吸收,该反应的离子方程式为______________ ;常温下,用100mL0.2mol·L-1InaOH溶液吸收448mL(标况)H2S气体,反应后溶液中离子浓度从大到小的顺序为__________________________________ 。
(5)25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子 (M2+),所需S2-最低浓度的对数值1gc(S2-)与Igc(M2+)的关系如右图所示,请回答:
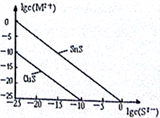
①25℃时Ksp(CuS)=_______________ 。
②25℃时向50mL的Sn2+、Cu2+浓度均为0.01mol/L的混合溶液中逐滴加入Na2S溶液,当Na2S溶液加到150mL时开始生成SnS沉淀,则此时溶液中Cu2+浓度为_____________ mol/L。
Ⅰ.COS(g)+H2(g)
 H2S(g)+CO(g) ΔH=X kJ·mol-1;
H2S(g)+CO(g) ΔH=X kJ·mol-1;I.CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-42 kJ·mol-1;
CO2(g)+H2(g) ΔH=-42 kJ·mol-1;(1)断裂1mol分子中的化学键所需吸收的能量如下表所示:
| 分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
| 能量/kJ·mol-1 | 1321 | 440 | 1076 | 680 | 930 | 1606 |
(2)向10 L容积不变的密闭容器中充入1mol COS(g)、1mol H2(g)和1mol H2O(g),进行上述两个反应,在某温度下达到平衡,此时CO的体积分数为4%,且测得此时COS的物质的量为0.80mol,则该温度下反应I的平衡常数为
(3)现有两个相同的2 L恒容绝热(与外界没有热量交换)密闭容器M、N,在M 中充入1mol CO和1molH2O,在N 中充入1molCO2和1molH2,均在700℃下开始按Ⅱ进行反应。达到平衡时,下列说法正确的是
A.两容器中CO 的物质的量M>N
B.两容器中正反应速率M
C.容器M 中CO的转化率与容器N 中CO2的转化率之和小于1
D.两容器中反应的平衡常数M>N
(4)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
| H2CO3 | H2S | |
| Ka1 | 4.4× 10-7 | 1.3×10-7 |
| Ka2 | 4.7× 10-11 | 7.1×10-15 |
(5)25℃时,用Na2S沉淀Cu2+、Sn2+两种金属离子 (M2+),所需S2-最低浓度的对数值1gc(S2-)与Igc(M2+)的关系如右图所示,请回答:

①25℃时Ksp(CuS)=
②25℃时向50mL的Sn2+、Cu2+浓度均为0.01mol/L的混合溶液中逐滴加入Na2S溶液,当Na2S溶液加到150mL时开始生成SnS沉淀,则此时溶液中Cu2+浓度为
18-19高三上·江西抚州·期末
类题推荐
CO是煤气的主要成分之一,H2S是许多煤化工产品的原料气。工业上,生产水煤气的主要反应如下:
Ⅰ.H2O(g)+C(s)=CO(g)+H2(g) △H=x kJ·mol-1
Ⅱ. CO(g)+H2O(g) H2(g)+CO2(g) △H =-41.2kJ • mol-1
H2(g)+CO2(g) △H =-41.2kJ • mol-1
(1)已知:2C(8)+O2(g)=2CO(g) △H =-220kJ • mol-1;利用下表中几种共价键的键能可以确定氢气
燃烧生成气态水的热化学反应方程式。
则H2O(g)+C(s)=CO(g)+H2(s) △H=___________ kJ·mol-1
(2)一定温度下,在1.0L密闭容器中放入1molC(s)、1molH2O(g)进行反应,反应时间(f)与容器内气体总压强(P)的数据如图:
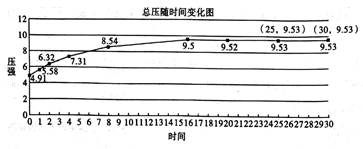
回答下列问题:
①下列事实能够说明该反应达到平衡状态的是________ (填序号)。
a.各反应物和生成物浓度相等 b.该反应的△H不变
c. v正(CO)=v逆(H2) d.混合气体的平均相对分子质量不变
②由图中数据计算,该反应的平衡常数K=___________ (精确到小数点后第二位)。
(3)现有两个体积相同的2L恒容密闭容器M、N,在M中充入1mol CO和1mol H2O,在N中充入1molCO2和1molH2,均在700℃下开始按Ⅱ进行反应,达到平衡时,容器M中CO的转化率α1与容器N中CO2的转化率α2的关系为________ (写数学表达式)。
(4)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
煤的气化过程中产生的H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为_______________ ;
常温下,用100mL 0.1mol·L-1NaOH溶液吸收224mL (标况)H2S气体,反应后溶液中的离子浓度由大到小的顺序为____________________ 。
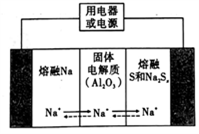
(5)硫化氢高温分解得到单质硫,钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池的总反应为2Na+xS Na2Sx(3,反应原理如图17所示;则电池放电时,正极反应式为:
Na2Sx(3,反应原理如图17所示;则电池放电时,正极反应式为:_____________________ 。
Ⅰ.H2O(g)+C(s)=CO(g)+H2(g) △H=x kJ·mol-1
Ⅱ. CO(g)+H2O(g)
 H2(g)+CO2(g) △H =-41.2kJ • mol-1
H2(g)+CO2(g) △H =-41.2kJ • mol-1(1)已知:2C(8)+O2(g)=2CO(g) △H =-220kJ • mol-1;利用下表中几种共价键的键能可以确定氢气
燃烧生成气态水的热化学反应方程式。
| 化学键 | O=O | H-H | O-H |
| 键能(kJ/mol) | 496 | 436 | 462 |
则H2O(g)+C(s)=CO(g)+H2(s) △H=
(2)一定温度下,在1.0L密闭容器中放入1molC(s)、1molH2O(g)进行反应,反应时间(f)与容器内气体总压强(P)的数据如图:

回答下列问题:
①下列事实能够说明该反应达到平衡状态的是
a.各反应物和生成物浓度相等 b.该反应的△H不变
c. v正(CO)=v逆(H2) d.混合气体的平均相对分子质量不变
②由图中数据计算,该反应的平衡常数K=
(3)现有两个体积相同的2L恒容密闭容器M、N,在M中充入1mol CO和1mol H2O,在N中充入1molCO2和1molH2,均在700℃下开始按Ⅱ进行反应,达到平衡时,容器M中CO的转化率α1与容器N中CO2的转化率α2的关系为
(4)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
| 电离平衡常数 | H2CO3 | H2S |
| Ka1 | 4.4×l0-7 | 1.3×l0-7 |
| Ka2 | 4.7×10-11 | 7. l×l0-15 |
煤的气化过程中产生的H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为
常温下,用100mL 0.1mol·L-1NaOH溶液吸收224mL (标况)H2S气体,反应后溶液中的离子浓度由大到小的顺序为
(5)硫化氢高温分解得到单质硫,钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,电池的总反应为2Na+xS
 Na2Sx(3,反应原理如图17所示;则电池放电时,正极反应式为:
Na2Sx(3,反应原理如图17所示;则电池放电时,正极反应式为:
H2S在金属离子的鉴定分析、煤化工等领域都有着重要应用。回答下列问题:
I.工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时还生成两种能参与大气循环的氧化物。
(1)该反应的化学方程式为___ 。
II.H2S可用于检测和沉淀金属阳离子。
(2)由H2S制得的水溶液为氢硫酸,向氢硫酸中滴加少量的硫酸铜溶液,溶液中
___ (填“增大”或“减小”)。
(3)已知:25℃时,Ksp(SnS)=1.0×10-25,Ksp(CdS)=8.0×10-27。该温度下,向浓度均为0.1mol·L-1的CdCl2和SnCl2的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=___ (溶液体积变化忽略不计)。
III.H2S是煤化工原料气脱硫过程的重要中间体,反应原理如下:
i.COS(g)+H2(g)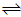 H2S(g)+CO(g) △H=+7kJ·mol-1;
H2S(g)+CO(g) △H=+7kJ·mol-1;
ii.CO(g)+H2O(g)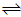 CO2(g)+H2(g) △H=-42kJ·mol-1。
CO2(g)+H2(g) △H=-42kJ·mol-1。
(4)已知:断裂1mol分子中的化学键所需吸收的能量如下表所示:
表中x=___ 。
(5)向10L溶积不变的密闭容器中充入1molCOS(g)、1molH2(g)和1molH2O(g),进行上述两个反应。
①随着温度升高,CO的平衡体积分数___ (填“增大”或“减小”),其原因是___ 。
②T1℃时,测得平衡时体系中COS的物质的量为0.80mol,CO的体积分数为5%。则该温度下,达到平衡时H2的物质的量为___ ;反应i的平衡常数为___ (保留两位有效数字)。
I.工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时还生成两种能参与大气循环的氧化物。
(1)该反应的化学方程式为
II.H2S可用于检测和沉淀金属阳离子。
(2)由H2S制得的水溶液为氢硫酸,向氢硫酸中滴加少量的硫酸铜溶液,溶液中
(3)已知:25℃时,Ksp(SnS)=1.0×10-25,Ksp(CdS)=8.0×10-27。该温度下,向浓度均为0.1mol·L-1的CdCl2和SnCl2的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=
III.H2S是煤化工原料气脱硫过程的重要中间体,反应原理如下:
i.COS(g)+H2(g)
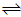 H2S(g)+CO(g) △H=+7kJ·mol-1;
H2S(g)+CO(g) △H=+7kJ·mol-1;ii.CO(g)+H2O(g)
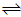 CO2(g)+H2(g) △H=-42kJ·mol-1。
CO2(g)+H2(g) △H=-42kJ·mol-1。(4)已知:断裂1mol分子中的化学键所需吸收的能量如下表所示:
| 分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
| 能量 | 1319 | 442 | x | 678 | 930 | 1606 |
(5)向10L溶积不变的密闭容器中充入1molCOS(g)、1molH2(g)和1molH2O(g),进行上述两个反应。
①随着温度升高,CO的平衡体积分数
②T1℃时,测得平衡时体系中COS的物质的量为0.80mol,CO的体积分数为5%。则该温度下,达到平衡时H2的物质的量为
H2S在重金属离子处理、煤化工等领域都有重要应用。请回答:
I.H2S是煤化工原料气脱硫过程的重要中间体,反应原理为:
i.COS(g)+H2(g) ⇌H2S(g)+CO(g) ∆H=+7kJ·mol
ii.CO(g)+H2O(g) ⇌CO2(g)+H2(g) ∆H=-42kJ·mol
已知断裂1mol气态分子中的化学键所需能量如下表所示。
(1)计算表中x=_______ ;
(2)T℃时,向VL容积不变的密闭容器中充入1molCOS(g)、1molH2(g)和1molH2O(g),发生上述两个反应。
①在T℃时测得平衡体系中COS为0.80mol,H2为0.85mol,则T℃时反应ⅰ的平衡常数K=____ (保留2位有效数字);
②上述反应达平衡后,若升高温度,则CO的平衡体积分数___ (填“增大”、“减小”或“不变”),其理由是___ ;
II.H2S在高温下分解制取H2,同时生成硫蒸气。
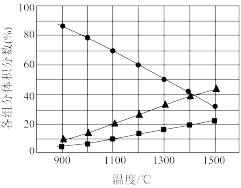
(3)向2L密闭容器中加入0.2molH2S,反应在不同温度(900~1500℃)下达到平衡时,混合气体中各组分的体积分数如下图所示,则在此温度区间内,H2S分解反应的主要化学方程式为__ ;在1300℃,反应经2min达到平衡,则0~2min的反应速率v(H2S)=___ 。
III.H2S用作重金属离子的沉淀剂。
(4)25℃时,向浓度均为0.001mol·L-1Sn2+和Ag+的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Ag+)=__ (已知:25℃时,Ksp(SnS)=1.0×10-25,Ksp(Ag2S)=1.6×10-49)。
I.H2S是煤化工原料气脱硫过程的重要中间体,反应原理为:
i.COS(g)+H2(g) ⇌H2S(g)+CO(g) ∆H=+7kJ·mol
ii.CO(g)+H2O(g) ⇌CO2(g)+H2(g) ∆H=-42kJ·mol
已知断裂1mol气态分子中的化学键所需能量如下表所示。
| 分子 | COS(g) | H2(g) | CO(g) | H2S(g) |
| 能量(kJ·mol-1) | 1310 | 442 | x | 669 |
(2)T℃时,向VL容积不变的密闭容器中充入1molCOS(g)、1molH2(g)和1molH2O(g),发生上述两个反应。
①在T℃时测得平衡体系中COS为0.80mol,H2为0.85mol,则T℃时反应ⅰ的平衡常数K=
②上述反应达平衡后,若升高温度,则CO的平衡体积分数
II.H2S在高温下分解制取H2,同时生成硫蒸气。
(3)向2L密闭容器中加入0.2molH2S,反应在不同温度(900~1500℃)下达到平衡时,混合气体中各组分的体积分数如下图所示,则在此温度区间内,H2S分解反应的主要化学方程式为

III.H2S用作重金属离子的沉淀剂。
(4)25℃时,向浓度均为0.001mol·L-1Sn2+和Ag+的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Ag+)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


