解答题-工业流程题 适中0.65 引用1 组卷410
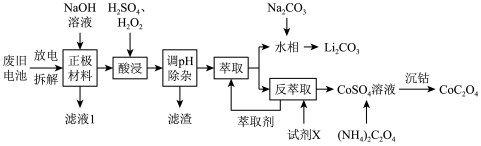
钴酸锂电池应用广泛,电池正极材料主要含有LiCoO2、导电剂乙炔黑、铝箔及少量Fe,可通过下列实验方法回收钴、锂。
几种金属离子沉淀完全(离子浓度为10-5mo/L)的pH如下表:
回答下列问题:
(1)LiCoO2中,Co元素的化合价为________ ,滤液I的主要成分是_________ 。
(2)已知:氧化性Co3+>H2O2>Fe3+,“酸浸”过程中H2O2所起主要作用是_________ 。“调节pH”除去的离子主要有Al3+和_________ 。
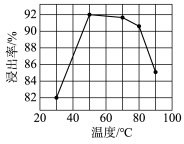
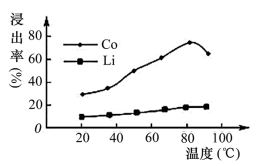
(3)酸浸时浸出率随温度变化如图所示,温度升高至50℃以上时漫出率下降的原因是___________ 。
(4)“萃取”和“反萃取”可简单表示为:Co2++2(HA)2 Co(HA2)2+2H+。则反萃取过程加入的试剂X是
Co(HA2)2+2H+。则反萃取过程加入的试剂X是_____________ 。
(5)向CoSO4溶液中加入NH4HCO3溶液,发生反应的离子方程式为____________ 。
(6)工业上用Li2CO3粗品制备高纯Li2CO3可采用如下方法将Li2CO3溶于盐酸,加入如图所示的电解槽,电解后向LiOH溶液中加入稍过量的NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
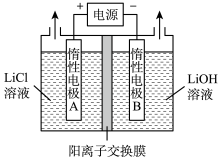
①电解槽中阳极的电极反应式是__________________ 。
②向LiOH溶液中加入稍过量的NH4HCO3溶液时,发生反应的化学方程式为__________ 。

几种金属离子沉淀完全(离子浓度为10-5mo/L)的pH如下表:
| 离子 | Fe3+ | Al3+ | Fe2+ | Co2+ |
| 溶液pH | 3.2 | 4.7 | 9.0 | 9.2 |
(1)LiCoO2中,Co元素的化合价为
(2)已知:氧化性Co3+>H2O2>Fe3+,“酸浸”过程中H2O2所起主要作用是
(3)酸浸时浸出率随温度变化如图所示,温度升高至50℃以上时漫出率下降的原因是

(4)“萃取”和“反萃取”可简单表示为:Co2++2(HA)2
(5)向CoSO4溶液中加入NH4HCO3溶液,发生反应的离子方程式为
(6)工业上用Li2CO3粗品制备高纯Li2CO3可采用如下方法将Li2CO3溶于盐酸,加入如图所示的电解槽,电解后向LiOH溶液中加入稍过量的NH4HCO3溶液,过滤、烘干得高纯Li2CO3。

①电解槽中阳极的电极反应式是
②向LiOH溶液中加入稍过量的NH4HCO3溶液时,发生反应的化学方程式为
2018·四川绵阳·二模
类题推荐
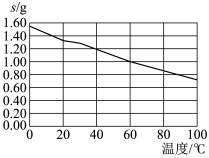
目前钴酸锂(LiCoO2)锂离子电池应用十分广泛,从废旧钴酸锂理离子电池中回收铝、铁、钴、锂等元素成了重要的研究课题,某小组模拟工业流程从废旧电池中对上述元素进行提取。

已知:①滤液1中阳离子有H+、CO3+、Fe3+、Al3+、Li+等;
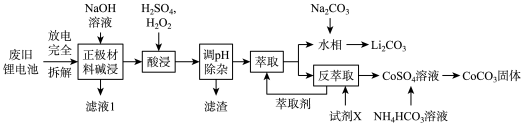
②几种物质不同温度下的溶解度如下表所示:
(1)钴酸锂(LiCoO2)中钴元素的化合价是_______________ 。
(2)上述流程中将CoO2-转化为Co3+的离子方程式为_________________ 。
(3)滤液1中加入Na2SO3的主要目的是_____________________ ;加入NaClO3的主要目的是____________ 。
(4)为了使Fe3+、Al3+沉淀完全(通常认为金属离子浓度小于或等于10-5mol·L-1时表示已沉淀完全)加入氨水调节pH的最小值是____________ (保留一位小数)。{已知:Ksp[Fe(OH)3]=1.0×10-39,Ksp[Al(OH)3]=2.7×10-34,lg3=0.52}

(5)滤液3中加入饱和Na2CO3溶液,过滤后,需要用“热水洗涤”的原因是_________ 。
(6)为得到高纯度的Li2CO3,需将粗产品Li2CO3与盐酸反应制得的LiCl进行电解。其原理如图所示:
①电解时阳极的电解反应式为_____________________ 。
②电解后向产品LiOH溶液中加入过滤NH4HCO3溶液生成Li2CO3,反应的化学方程式为__________ 。

已知:①滤液1中阳离子有H+、CO3+、Fe3+、Al3+、Li+等;
②几种物质不同温度下的溶解度如下表所示:
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)钴酸锂(LiCoO2)中钴元素的化合价是
(2)上述流程中将CoO2-转化为Co3+的离子方程式为
(3)滤液1中加入Na2SO3的主要目的是
(4)为了使Fe3+、Al3+沉淀完全(通常认为金属离子浓度小于或等于10-5mol·L-1时表示已沉淀完全)加入氨水调节pH的最小值是

(5)滤液3中加入饱和Na2CO3溶液,过滤后,需要用“热水洗涤”的原因是
(6)为得到高纯度的Li2CO3,需将粗产品Li2CO3与盐酸反应制得的LiCl进行电解。其原理如图所示:
①电解时阳极的电解反应式为
②电解后向产品LiOH溶液中加入过滤NH4HCO3溶液生成Li2CO3,反应的化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

 Co(HA2)2+2H+,则反萃取过程加入的试剂X是
Co(HA2)2+2H+,则反萃取过程加入的试剂X是