解答题-原理综合题 适中0.65 引用2 组卷259
目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行了探究。已知在不同温度下的化学平衡常数(K1、K2、K3)如表所示。
请回答下列问题:
(1)反应②是_______ (填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______ (用K1、K2表示);根据反应③判断△S_______ (填“>”“=”或“<”)0,在_______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有______ (填字母,后同)。
A.缩小反应容器的容积 B.增大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为 0.1mol/L、0.8 mol/L、0.3 mol/L、0.15 mol/L,则此时υ(正)_______ υ(逆) (填“>”“=”或“<”)。
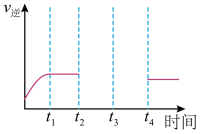
(5)某兴趣小组研究反应②的逆反应速率在下列不同条件下随时间的变化曲线,开始时升高温度,t1时平衡,t2时减小压强,t3时增大CO的浓度,t4时又达到平衡。在下图中画出t2至t4的曲线。_____
| 化学反应 | 焓变 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |||
| ①2H2(g)+CO(g) | △H1 | K1 | 2.5 | 0.34 | 0.15 |
| ②CO2(g)+H2(g)⇌CO(g)+H2O(g) | △H2 | K2 | 1.0 | 1.70 | 2.52 |
| ③CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) | △H3 | K3 | |||
(1)反应②是
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有
A.缩小反应容器的容积 B.增大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为 0.1mol/L、0.8 mol/L、0.3 mol/L、0.15 mol/L,则此时υ(正)
(5)某兴趣小组研究反应②的逆反应速率在下列不同条件下随时间的变化曲线,开始时升高温度,t1时平衡,t2时减小压强,t3时增大CO的浓度,t4时又达到平衡。在下图中画出t2至t4的曲线。

17-18高二上·河南南阳·阶段练习
类题推荐
前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三个化学反应原理进行探究。已知在不同温度下的化学平衡常数(K1、K2、K3)如表所示。请回答下列问题:
(1)反应②是__________ (填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=__________ (用K1、K2表示);反应③的∆S__________ (填“>”“<”或“=”)0,在__________ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)500℃时,某时刻测得反应③中CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol/L、0.8mol/L、0.3mol/L、0.15mol/L,则此时v(正)__________ (填“>”“=”或“<”)v(逆)。
(4)根据上述表格测得焓变,下列能量关系图合理的是__________ (填标号)。
A.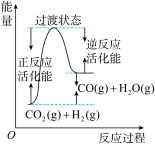 B.
B.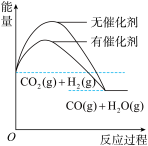
C.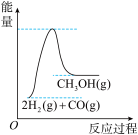 D.
D.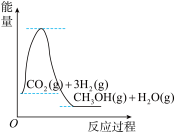
| 化学反应 | 焓变 | 平衡常数 | 温度 | ||
| 500/℃ | 700/℃ | 800/℃ | |||
| ①2H2(g)+CO(g)⇌CH3OH(g) | ∆H1 | K1 | 2.5 | 0.34 | 0.15 |
| ②2CO2(g)+H2(g)⇌H2O(g)+CO(g) | ∆H2 | K2 | 1.0 | 1.70 | 2.52 |
| ③CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) | ∆H3 | K3 | |||
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(3)500℃时,某时刻测得反应③中CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol/L、0.8mol/L、0.3mol/L、0.15mol/L,则此时v(正)
(4)根据上述表格测得焓变,下列能量关系图合理的是
A.
 B.
B.
C.
 D.
D.
目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究。已知在不同温度下的化学反应平衡常数(K1、K2、K3)如表所示。请回答下列问题:
(1)反应②是____ (填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=____ (用K1、K2表示);根据反应③判断ΔS___ 0(填“>”、“=”或“<”),在____ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol/L、0.8mol/L、0.3mol/L、0.15mol/L,则此时v(正)___ v(逆)(填“>”、“=”或“<”)。
(4)根据上述表格测得焓变,下列能量关系图合理的是_____
A.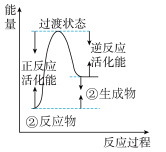 B.
B.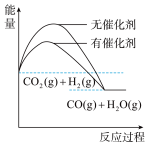 C.
C.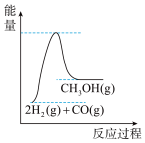 D.
D.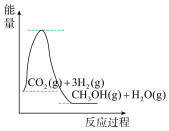
| 化学反应 | 焓变 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |||
| ①2H2(g)+CO(g) | ΔH1 | K1 | 2.5 | 0.34 | 0.15 |
| ②CO2(g)+H2(g) | ΔH2 | K2 | 1.0 | 1.70 | 2.52 |
| ③CO2(g)+3H2(g) | ΔH3 | K3 | |||
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol/L、0.8mol/L、0.3mol/L、0.15mol/L,则此时v(正)
(4)根据上述表格测得焓变,下列能量关系图合理的是
A.
 B.
B. C.
C. D.
D.
目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究。已知在不同温度下的化学反应平衡常数(K1、K2、K3)如下表所示:
请回答下列问题:
(1)反应②是________ (填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=________ (用K1、K2表示);根据反应③判断ΔS___ 0(填“>”、“=”或“<”),在______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol/L、0.8mol/L、0.3mol/L、0.15mol/L,则此时v正________ v逆(填“>”、“=”或“<”)。
| 化学反应 | 焓变 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | ΔH1 | K1 | 2.5 | 0.34 | 0.15 |
②CO2(g)+H2(g) CO(g)+H2O(g) CO(g)+H2O(g) | ΔH2 | K2 | 1.0 | 1.70 | 2.52 |
③CO2(g)+3H2(g) CH3OH(g)+H2O(g) CH3OH(g)+H2O(g) | ΔH3 | K3 | |||
请回答下列问题:
(1)反应②是
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(3)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol/L、0.8mol/L、0.3mol/L、0.15mol/L,则此时v正
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


