单选题 适中0.65 引用3 组卷233
废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH4+完全转化为N2,该反应可表示为2NH4++3ClO-=N2↑+3Cl-+2H++3H2O。下列说法中,不正确的是
| A.反应中氮元素被氧化,氯元素被还原 |
| B.还原性NH4+< Cl- |
| C.反应中每生成1 mol N2,转移6 mol电子 |
| D.经此法处理过的废水不可以直接排放 |
17-18高一上·北京·期中
类题推荐
处理含氰(CN-)废水涉及以下反应,其中无毒的OCN-中碳元素为+4价。
CN-+OH-+Cl2→OCN-+Cl-+H2O(未配平) 反应Ⅰ
2OCN-+4OH-+3Cl2=2CO2+N2+6Cl-+2H2O 反应Ⅱ
下列说法中正确的是
CN-+OH-+Cl2→OCN-+Cl-+H2O(未配平) 反应Ⅰ
2OCN-+4OH-+3Cl2=2CO2+N2+6Cl-+2H2O 反应Ⅱ
下列说法中正确的是
| A.反应I中碳元素被还原 |
| B.反应II中CO2为氧化产物 |
| C.处理过程中,每产生1 mol N2,消耗3 molCl2 |
| D.处理I中CN-与Cl2按物质的量比例1:1进行反应 |
微生物电解法可用于处理工业废水,其工作原理如同所示,下列说法不正确的是
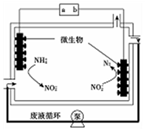

| A.左测电极反应式是2H2O+NH4+-6e-=NO2-+8H+ |
| B.在微生物作用下,废水中的NH4+最终转化为N2 |
| C.a是电池的正极,b是电池的负极 |
| D.处理0.5 mol NH4+,经过溶液中电子的物质的量是3 mol |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


