解答题-结构与性质 适中0.65 引用1 组卷120
已知元素X、Y、Z、R为前四周期元素,且原子序数依次增大。X原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态。请回答下列问题:
(1)R基态原子的外围电子排布式为____ ,其基态原子有__ 种能量不同的电子。
(2)元素X、Y、Z的第一电离能由小到大的顺序为(用元素符号表示)____ 。
(3)与XYZ-互为等电子体微粒的化学式为______ (写出一种即可),XYZ-的中心原子的杂化方式为_____ 。
(4)R2+与NH3形成的配离子中,提供孤对电子的原子是__ 。
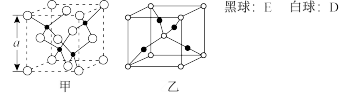
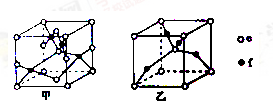
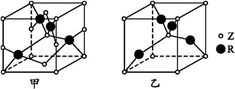
(5)已知Z、R能形成两种化合物,其晶胞如图所示,甲的化学式为__ ,乙的化学式为__ ;高温时,甲易转化为乙的原因为_____________ 。
(6)若甲晶体中一个晶胞的边长为a pm,则甲晶体的密度为______ g·cm-3(写出含a的表达式,用NA表示阿伏伽德罗常数的值)。
(1)R基态原子的外围电子排布式为
(2)元素X、Y、Z的第一电离能由小到大的顺序为(用元素符号表示)
(3)与XYZ-互为等电子体微粒的化学式为
(4)R2+与NH3形成的配离子中,提供孤对电子的原子是
(5)已知Z、R能形成两种化合物,其晶胞如图所示,甲的化学式为
(6)若甲晶体中一个晶胞的边长为a pm,则甲晶体的密度为

17-18高三上·内蒙古巴彦淖尔·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网