填空题 适中0.65 引用1 组卷838
化学反应过程中,不仅有物质的变化,同时还伴随有能量的变化。
(1)已知几种化学键的键能如表所示:
则反应Cl2(g)+ 3F2(g) 2ClF3(g) 的△H=
2ClF3(g) 的△H=_____________ kJ·mol—1 。
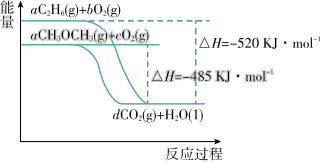
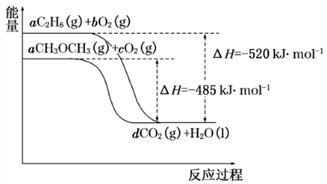
(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。
请回答下列问题:
①乙烷的燃烧热ΔH=____ kJ·mol-1。
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量__ (填“多”或“少”)。
③根据题图写出二甲醚完全燃烧时的热化学方程式_____________ 。
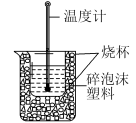
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量____ (填“相等”或“不相等”,忽略实验本身误差,下同),所求中和热_____ (填“相等”或“不相等”,)。
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会___ (填“偏大”“偏小”或“无影响”)。
(1)已知几种化学键的键能如表所示:
| 化学键 | Cl—Cl | F—F | Cl—F |
| 键能/ kJ·mol—1 | 242 | 159 | 172 |
则反应Cl2(g)+ 3F2(g)
 2ClF3(g) 的△H=
2ClF3(g) 的△H=(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。

请回答下列问题:
①乙烷的燃烧热ΔH=
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量
③根据题图写出二甲醚完全燃烧时的热化学方程式
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会
17-18高二上·广东·期中
类题推荐
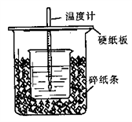
Ⅰ.50mL0.5mol·L-1的盐酸与50mL0.55mol·L-1的NaOH溶液在下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,可知下图装置有三处不妥之处,请指出____________________
(2)在测定中和热的实验中,计算反应热时需要的数据有________________
①酸的浓度和体积 ②碱的浓度和体积 ③比热容
④反应前后溶液的温度差 ⑤操作所需时间
A.①②③⑤ B. ①②③④ C. ②③④⑤ D. ①③④⑤
(3)实验中改用60mL0.50mol·L-1的盐酸跟50mL0.55mol·L-1的NaOH溶液进行反应,与上述实验相比,所求中和热_______ (填“相等”或“不相等”),所放出的热量____ (填“相等”或“不相等”)
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会_____ (填“偏大”、“偏小”或“无影响”).
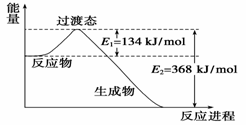
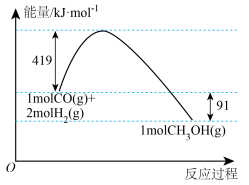
Ⅱ.甲醇是重要的工业原料。煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g) CH3OH(g)。已知:①下图为反应的能量变化和物质键能
CH3OH(g)。已知:①下图为反应的能量变化和物质键能
②CO(g)+1/2O2(g)===CO2(g) ΔH=-280kJ/mol
H2(g)+1/2O2(g)===H2O(l) ΔH=-284kJ/mol
H2O(l)===H2O(g) ΔH=+ 44kJ/mol
请回答下列问题:
(1)请写出表示气态甲醇燃烧热的热化学方程式_________________________ 。
(2)H—O键的键能x为_________ kJ/mol。
(3)甲醇气体分解为CO和H2两种气体的反应的活化能为_________ kJ/mol。

(1)从实验装置上看,可知下图装置有三处不妥之处,请指出
(2)在测定中和热的实验中,计算反应热时需要的数据有
①酸的浓度和体积 ②碱的浓度和体积 ③比热容
④反应前后溶液的温度差 ⑤操作所需时间
A.①②③⑤ B. ①②③④ C. ②③④⑤ D. ①③④⑤
(3)实验中改用60mL0.50mol·L-1的盐酸跟50mL0.55mol·L-1的NaOH溶液进行反应,与上述实验相比,所求中和热
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
Ⅱ.甲醇是重要的工业原料。煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)
 CH3OH(g)。已知:①下图为反应的能量变化和物质键能
CH3OH(g)。已知:①下图为反应的能量变化和物质键能| 化学键 | H-H | H-O | O=O |
| 键能kJ/mol | 436 | x | 496 |

②CO(g)+1/2O2(g)===CO2(g) ΔH=-280kJ/mol
H2(g)+1/2O2(g)===H2O(l) ΔH=-284kJ/mol
H2O(l)===H2O(g) ΔH=+ 44kJ/mol
请回答下列问题:
(1)请写出表示气态甲醇燃烧热的热化学方程式
(2)H—O键的键能x为
(3)甲醇气体分解为CO和H2两种气体的反应的活化能为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网