解答题-实验探究题 适中0.65 引用1 组卷134
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。以卤块为原料可制得轻质氧化镁,工艺流程如图:
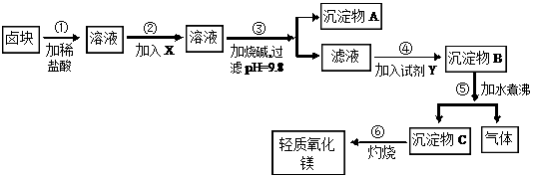
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1和表2提供的资料,填写空白:
(1)在步骤②中加入的试剂X(从表2中选择)是_______ 而不是双氧水,其原因是_______________________ 。写出加入X发生反应的离子方程式_______________________ 。
(2)在步骤③中控制pH=9.8,其目的是____________________________ 。
(3)沉淀物A的成分为______________ ,试剂Y(从表2中选择)应该是_______ 。
(4)在步骤⑤中发生反应的化学方程式是________________________ 。
(5)若在实验室中完成步骤⑥,则沉淀物C必需在_______ (填仪器名称)中灼烧。

已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1和表2提供的资料,填写空白:
| 表1 生成氢氧化物沉淀的pH | 表2 化学试剂价格表 | ||||
| 物质 | 开始沉淀 | 沉淀完全 | 试剂 | 价格(元/吨) | |
| Fe(OH)3 | 2.7 | 3.7 | 漂液(含25.2% NaClO) | 450 | |
| Fe(OH)2 | 7.6 | 9.6 | 双氧水(含30% H2O2) | 2400 | |
| Mn(OH)2 | 8.3 | 9.8 | 烧碱(含98% NaOH) | 2100 | |
| Mg(OH)2 | 10.0 | 11.1 | 纯碱(含99.5% Na2CO3) | 600 | |
(1)在步骤②中加入的试剂X(从表2中选择)是
(2)在步骤③中控制pH=9.8,其目的是
(3)沉淀物A的成分为
(4)在步骤⑤中发生反应的化学方程式是
(5)若在实验室中完成步骤⑥,则沉淀物C必需在
17-18高二上·山西吕梁·期中
类题推荐
卤块的主要成分是MgCl 2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
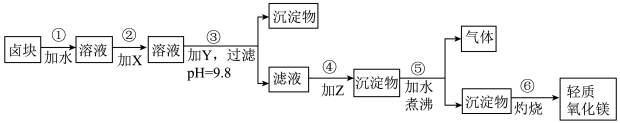
表1
﹡Fe2+氢氧化物呈絮状,不易从溶液中除去,必须将它氧化后以Fe(OH)3沉淀形式才能除尽
表2
若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,回答下列问题:
(1)步骤②中加入的试剂X,最佳选择_____________ (填物质名称),其作用是___________________ 。
(2)步骤③生成的沉淀物含有____________________ (填化学式)。
(3)步骤⑤中发生反应的化学方程式为_____________________________ 。
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是铁三脚、酒精喷灯、________ 和泥三角。
(5)在实验室中,为了除去MgCl 2酸性溶液中的Fe3+而得到较纯净的MgCl2溶液,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸,这种试剂是____________ (填字母)。
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3

表1
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
﹡Fe2+氢氧化物呈絮状,不易从溶液中除去,必须将它氧化后以Fe(OH)3沉淀形式才能除尽
表2
| 物质 | 价格(元/吨) |
| 漂白液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
若要求产品尽量不含杂质,而且生产成本较低,根据表1和表2提供的资料,回答下列问题:
(1)步骤②中加入的试剂X,最佳选择
(2)步骤③生成的沉淀物含有
(3)步骤⑤中发生反应的化学方程式为
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是铁三脚、酒精喷灯、
(5)在实验室中,为了除去MgCl 2酸性溶液中的Fe3+而得到较纯净的MgCl2溶液,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸,这种试剂是
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子的易溶盐。以卤块为原料可制得轻质氧化镁,工艺流程如图
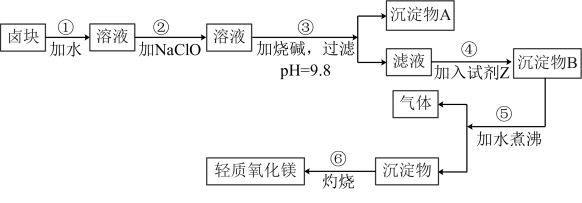
已知:(1)Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(2)原料价格表
(3)生成氢氧化物沉淀的PH
回答下列问题:
(1)某课外兴趣小组设计实验证明卤块中含有Fe3+为:取少许样品加水溶解,____ ,则说明卤块中含Fe3+。
(2)工业上冶炼镁常用的方法的化学方程式为____ 。
(3)步骤②加入NaClO而不用H2O2的原因是____ ,步骤②反应后产生少量红褐色沉淀,该反应中氧化剂与还原剂的比例为____ 。
(4)沉淀A的主要成分为____ ;步骤④加入的物质为____ 。
(5)步骤⑤发生的反应的化学方程式为____ 。
(6)步骤⑥如在实验室进行,应选用在____ (填仪器名称)中灼烧。

已知:(1)Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(2)原料价格表
| 物质 | 价格/(元·吨-1) |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
(1)某课外兴趣小组设计实验证明卤块中含有Fe3+为:取少许样品加水溶解,
(2)工业上冶炼镁常用的方法的化学方程式为
(3)步骤②加入NaClO而不用H2O2的原因是
(4)沉淀A的主要成分为
(5)步骤⑤发生的反应的化学方程式为
(6)步骤⑥如在实验室进行,应选用在
卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
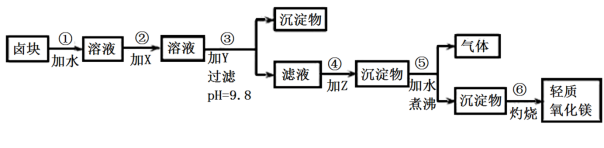
若要求产品尽量不含杂质,而且生产成本较低,根据表 1 和表 2 提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
表2原料价格表
*Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(1)卤块加水过程中能够增大溶解效率的措施有________ 、__________ (任意写两点)
(2)在步骤②中加入的试剂 X,最佳的选择是_________ ,其作用是 ________ 。
(3)在步骤③之所以要控制 pH=9.8,其目的是__________________ 。
(4)在步骤④中加入的试剂 Z 应是_________________ ;
(5)在步骤⑤中发生的反应是________ 。
(6)在实验室中,为了除去 MgCl2酸性溶液中的 Fe3+而得到较纯净的MgCl2溶液,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸。这种试剂是_____________ 。
A、NH3·3 H2O B、NaOH C、Na2CO3 D、MgCO3
(7)已知 298K 时,Mg(OH)2的溶度积常数为 Ksp=5.6×10-12,取适量MgCl2溶液,加入一定量的烧碱溶液达到沉淀平衡,测得pH=13,则所得溶液中的 c(Mg2+)=______ mol/L。

若要求产品尽量不含杂质,而且生产成本较低,根据表 1 和表 2 提供的资料,填写空白:
表1生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 完全沉淀 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6* |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2原料价格表
| 物质 | 价格(元·吨-1) |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
*Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(1)卤块加水过程中能够增大溶解效率的措施有
(2)在步骤②中加入的试剂 X,最佳的选择是
(3)在步骤③之所以要控制 pH=9.8,其目的是
(4)在步骤④中加入的试剂 Z 应是
(5)在步骤⑤中发生的反应是
(6)在实验室中,为了除去 MgCl2酸性溶液中的 Fe3+而得到较纯净的MgCl2溶液,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适量的盐酸。这种试剂是
A、NH3·3 H2O B、NaOH C、Na2CO3 D、MgCO3
(7)已知 298K 时,Mg(OH)2的溶度积常数为 Ksp=5.6×10-12,取适量MgCl2溶液,加入一定量的烧碱溶液达到沉淀平衡,测得pH=13,则所得溶液中的 c(Mg2+)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


