单选题 适中0.65 引用4 组卷199
发射“神六“时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。
已知:N2(g) + 2O2(g) = 2NO2(g); △H = + 67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g); △H = – 534kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是
已知:N2(g) + 2O2(g) = 2NO2(g); △H = + 67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g); △H = – 534kJ/mol
下列关于肼和NO2反应的热化学方程式中,正确的是
| A.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(l);△H = – 1135.7kJ/mol |
| B.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H = – 1000.3kJ/mol |
| C.N2H4(g) + NO2(g) =3/2N2(g) + 2H2O(l);△H = – 568.35kJ/mol |
| D.2N2H4(g) + 2NO2(g) = 3N2(g) + 4H2O(g);△H = – 1135.7kJ/mol |
17-18高三上·山西大同·阶段练习
类题推荐
我国发射“神五”所用的长征2号火箭的主要燃料是偏二甲肼(C2H8N2),氧化剂是NO2,燃烧产物只有N2、CO2和H2O。有的国家用肼(N2H4)作为火箭发动机的燃料。NO2为氧化剂,反应生成N2和水蒸气。已知:
①N2(g)+2O2(g) === 2NO2(g) △H=+67.7kJ• mol-1,
②N2H4(g)+O2(g) === N2(g)+ 2H2O(g) △H=" -534" kJ• mol-1。
下列关于肼和NO2反应的热化学方程式中正确的是
①N2(g)+2O2(g) === 2NO2(g) △H=+67.7kJ• mol-1,
②N2H4(g)+O2(g) === N2(g)+ 2H2O(g) △H=" -534" kJ• mol-1。
下列关于肼和NO2反应的热化学方程式中正确的是
| A.2N2H4(g)+2NO2(g) === 3N2(g) + 4H2O (l)△H=" -1135.7" kJ• mol-1 |
| B.2N2H4(g)+2NO2(g) ===2N2(g) +4H2O(l)△H=" -1135.7" kJ• mol-1 |
C.N2H4(g)+NO2(g) ===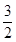 N2(g) +2H2O(g )△H=" -1135.7" kJ• mol-1 N2(g) +2H2O(g )△H=" -1135.7" kJ• mol-1 |
| D.2N2H4(g) + 2NO2(g) ===3N2(g)+4 H2O (g)△H=" -1135.7" kJ• mol-1 |
我国采用长征三号甲运载火箭成功发射了 “嫦娥一号” 卫星。肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气。已知:N2(g)+2O2(g)=N2O4(g) △H =+8.7kJ/mol,N2H4(g)+O2(g)=N2(g)+2H2O(g) △H= -534kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是 ( )
下列表示肼和N2O4反应的热化学方程式,正确的是 ( )
| A.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(l) △H=–1059.3 kJ/mo |
| B.N2H4(g) + |
| C.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–542.7 kJ/mol |
| D.2N2H4(g) + N2O4(g) = 3N2(g) + 4H2O(g) △H=–1076.7 kJ/mol |
肼(N2H4)是火箭发动机的燃料,它与N2O4反应生成氮气和水蒸气。已知:
①N2(g)+2O2(g)=N2O4(g) △H=+8.7 kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H= - 534.0 kJ/mol
下列表示肼跟N2O4反应的热化学方程式正确的是
①N2(g)+2O2(g)=N2O4(g) △H=+8.7 kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g) △H= - 534.0 kJ/mol
下列表示肼跟N2O4反应的热化学方程式正确的是
| A.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-542.7 kJ/mol |
| B.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-1076.7 kJ/mol |
| C.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-2153.4 kJ/mol |
| D.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) △H=-1059.3 kJ/mol |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


