解答题-原理综合题 适中0.65 引用1 组卷100
已知某反应的平衡常数表达式为:K= 其平衡常数随温度变化如下表所示:请回答下列问题:
其平衡常数随温度变化如下表所示:请回答下列问题:
(1)该反应的ΔH______ 0(填“>”或“<”)。
(2)若在500 ℃时进行上述反应,某时刻测得四种物质的体积分数彼此相等,则此时反应_____ 向进行中(“正”或“逆”);
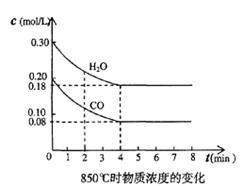
(3)850 ℃时在一个固定体(反应器中,投入2 molCO和3 molH2O(g),发生上述反应,CO和H2O(g)的浓度变化如图所示,则
①4 min时H2的物质的量分数=___________ ;②K1=_____________ ;
③若4分钟时测得反应的热效应数值为a kJ,则该反应的热化学方程式为:_________ ;
④若第6分钟将容器压缩为5L,画出6~8分钟CO的浓度变化图象(注明起点坐标)______________ ;
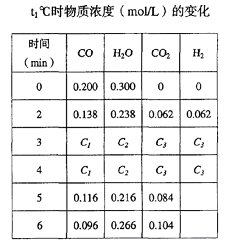
(4)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度随时间变化如下表。
①3~4min时,v正________ v逆(填“>”或“=”或“<”),C1 ____ 0.08 mol/L(填“>”或“=”或“<”);
②反应在4 min~5 min,平衡向逆方向移动,可能的原因是_________ (单选),反应在5 min~6 min,平衡向正方向移动,可能的原因是___________ (单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | K1 |
(1)该反应的ΔH
(2)若在500 ℃时进行上述反应,某时刻测得四种物质的体积分数彼此相等,则此时反应
(3)850 ℃时在一个固定体(反应器中,投入2 molCO和3 molH2O(g),发生上述反应,CO和H2O(g)的浓度变化如图所示,则

①4 min时H2的物质的量分数=
③若4分钟时测得反应的热效应数值为a kJ,则该反应的热化学方程式为:
④若第6分钟将容器压缩为5L,画出6~8分钟CO的浓度变化图象(注明起点坐标)
(4)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度随时间变化如下表。

①3~4min时,v正
②反应在4 min~5 min,平衡向逆方向移动,可能的原因是
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
17-18高二上·四川成都·阶段练习
类题推荐
(1)化学平衡常数K表示可逆反应进行程度,K值越大,表示_________________ ,K值大小与温度的关系是:△H<0(正反应放热),当温度升高K值______________ 。
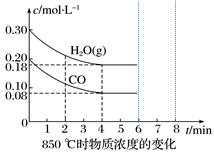
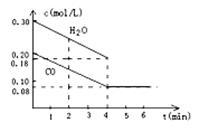
(2)在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g) + H2O(g) CO2(g)+H2(g) △H<0,CO和H2O浓度变化如下图所示,则0~4min的平均速率v(CO)=
CO2(g)+H2(g) △H<0,CO和H2O浓度变化如下图所示,则0~4min的平均速率v(CO)=_________ 。
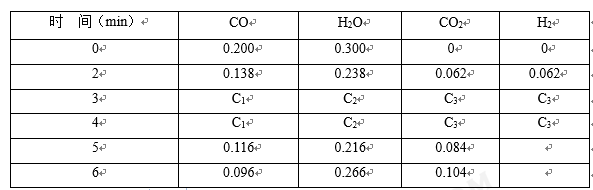
(3)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表。
t1℃时物质浓度(mol/L)的变化
①表中3~4min反应处于___________ 状态;c1数值_________ 0.08mol/L(填“>”“<”“=”)
②反应在4~5min,平衡向逆方向移动,可能的原因是_______ (单选),表中5~6min数值发生变化,可能的原因是_________ (单选)
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
(2)在一体积为10L的容器中,通入一定量的CO和H2O(g),在850℃时发生如下反应:CO(g) + H2O(g)
 CO2(g)+H2(g) △H<0,CO和H2O浓度变化如下图所示,则0~4min的平均速率v(CO)=
CO2(g)+H2(g) △H<0,CO和H2O浓度变化如下图所示,则0~4min的平均速率v(CO)=
(3)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表。
t1℃时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①表中3~4min反应处于
②反应在4~5min,平衡向逆方向移动,可能的原因是
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0。CO和H2O的浓度变化如图所示。
CO2(g)+H2(g) ΔH<0。CO和H2O的浓度变化如图所示。
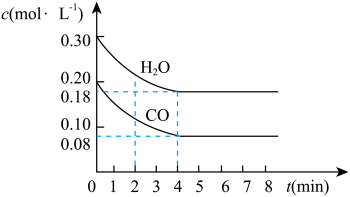
请解答下列各题:
(1)0~4min内的平均反应速率v(CO)=___ mol/(L·min),v(H2)=___ mol/(L·min),v(CO2)=___ mol/(L·min)。
(2)请你在图中标出CO2和H2的浓度变化。___
(3)T℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表。
①表中3min~4min之间,反应处于___ 状态;c1___ 0.08mol/L(填“大于”、“小于”或“等于”)。
②反应在4min~5min之间,平衡向逆反应方向移动,可能的原因是___ (单选),表中5min~6min之间数值发生变化,可能的原因是___ (单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
 CO2(g)+H2(g) ΔH<0。CO和H2O的浓度变化如图所示。
CO2(g)+H2(g) ΔH<0。CO和H2O的浓度变化如图所示。
请解答下列各题:
(1)0~4min内的平均反应速率v(CO)=
(2)请你在图中标出CO2和H2的浓度变化。
(3)T℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表。
| 时间(min) | 0 | 2 | 3 | 4 | 5 | 6 |
| CO | 0.200 | 0.138 | c1 | c1 | 0.116 | 0.096 |
| H2O | 0.300 | 0.238 | c2 | c2 | 0.216 | 0.266 |
| CO2 | 0 | 0.062 | c3 | c3 | 0.084 | 0.104 |
| H2 | 0 | 0.062 | c4 | c4 |
②反应在4min~5min之间,平衡向逆反应方向移动,可能的原因是
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 CO2(g)+H2(g) ΔH>0请回答下列问题:
CO2(g)+H2(g) ΔH>0请回答下列问题: