解答题-原理综合题 适中0.65 引用1 组卷289
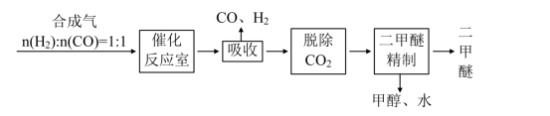
二甲醚(CH3OCH3)是一种清洁、高效、具有优良的环保性能的可燃物,被称为21世纪的新型能。工业制备二甲醚的生产流程如下:
催化反应室中(压力2.0~10.0MPa,温度300℃)进行下列反应:
(Ⅰ)CO(g)+2H2(g) CH3OH(g) ΔH1=-90.7kJ·mol-1
CH3OH(g) ΔH1=-90.7kJ·mol-1
(Ⅱ)2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol-1
(Ⅲ)CO(g)+H2O(g) CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1
CO2(g)+H2(g) ΔH3=-41.2kJ·mol-1
(1)催化反应室中的总反应:3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)
CH3OCH3(g)+CO2(g)
①该反应的反应热△H=__________ 。
②催化反应室中采用300℃的反应温度,理由是______________________________ 。
(2)已知:反应(Ⅰ)在300℃时的化学平衡常数为0.27。该温度下将2molCO、3molH2和2molCH3OH充入容积为2L的密闭容器中,此时反应将__________ (填“正向进行”、“逆向进行”或“处于平衡状态”)。
(3)上述流程中二甲醚精制的实验操作名称为____________________ 。
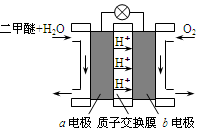
(4)如图为绿色电“二甲醚燃料电池”的工作原理示意图。
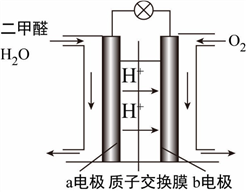
①该电池工作时,H+向__________ 极移动(填“正”或“负”);
②a电极的电极反应式为________________________________________ 。
催化反应室中(压力2.0~10.0MPa,温度300℃)进行下列反应:
(Ⅰ)CO(g)+2H2(g)
(Ⅱ)2CH3OH(g)
(Ⅲ)CO(g)+H2O(g)
(1)催化反应室中的总反应:3CO(g)+3H2(g)
①该反应的反应热△H=
②催化反应室中采用300℃的反应温度,理由是
(2)已知:反应(Ⅰ)在300℃时的化学平衡常数为0.27。该温度下将2molCO、3molH2和2molCH3OH充入容积为2L的密闭容器中,此时反应将
(3)上述流程中二甲醚精制的实验操作名称为
(4)如图为绿色电“二甲醚燃料电池”的工作原理示意图。

①该电池工作时,H+向
②a电极的电极反应式为
17-18高三上·北京朝阳·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 CH3OH(g) ΔH=-90.7 kJ/mol
CH3OH(g) ΔH=-90.7 kJ/mol

 CH3OH(g)ΔH=-90.7 kJ/mol ①
CH3OH(g)ΔH=-90.7 kJ/mol ①
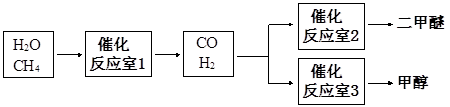
 CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示,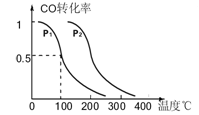
 CO(g)+2H2(g)的平衡常数为
CO(g)+2H2(g)的平衡常数为