解答题-实验探究题 适中0.65 引用2 组卷168
三盐基硫酸铅(3PbO·PbSO4·H2O)简称三盐,白色或微黄色粉末,稍带甜味、有毒。200℃以上开始失去结晶水,不溶于水及有机溶剂。可用作聚氯乙烯的热稳定剂。以铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。
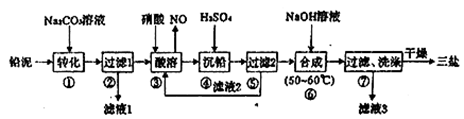
已知:常温下PbSO4的溶解度比PbCO3的溶解度大
请回答下列问题:
(1)步骤①转化的目的是____________ ,滤液1中的溶质为Na2CO3和_________ (填化学式)。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是___________ (任写一条)。其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为__________________ 。
(3)滤液2中可循环利用的溶质为__________ (填化学式)。
(4)步骤⑥合成三盐的化学方程式为_______________________________________ (已知反应中元素价态不变)。
(5)简述步骤⑦洗涤沉淀的方法__________________________________________ 。

已知:常温下PbSO4的溶解度比PbCO3的溶解度大
请回答下列问题:
(1)步骤①转化的目的是
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是
(3)滤液2中可循环利用的溶质为
(4)步骤⑥合成三盐的化学方程式为
(5)简述步骤⑦洗涤沉淀的方法
17-18高三上·吉林长春·期中
类题推荐
三盐 可用作聚氯乙烯的热稳定剂,
可用作聚氯乙烯的热稳定剂, 以上开始失去结晶水,不溶于水及有机溶剂。以铅泥
以上开始失去结晶水,不溶于水及有机溶剂。以铅泥 主要成分为PbO、Pb及
主要成分为PbO、Pb及 等
等 为原料制备三盐的工艺流程如图所示。
为原料制备三盐的工艺流程如图所示。
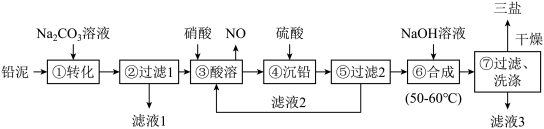
已知: 和
和 的溶解度和溶度积Ksp如下表。
的溶解度和溶度积Ksp如下表。
(1)步骤 转化的目的是
转化的目的是___ ,滤液1中的溶质为 和
和____  填化学式
填化学式 。
。
(2)步骤 酸溶时,为提高酸溶速率,可采取的措施是
酸溶时,为提高酸溶速率,可采取的措施是____  任写一条
任写一条 。其中铅与硝酸反应生成
。其中铅与硝酸反应生成 和NO的离子方程式为
和NO的离子方程式为_______ 。
(3)滤液2中可循环利用的溶质的化学式为____ 。若步骤 沉铅后的滤液中
沉铅后的滤液中 ,则此时
,则此时
_____  。
。
(4)步骤 合成三盐的化学方程式为
合成三盐的化学方程式为__________________ 。

已知:
| 化合物 | ||
| 溶解度 | ||
| Ksp |
(1)步骤
(2)步骤
(3)滤液2中可循环利用的溶质的化学式为
(4)步骤
三盐(3PbO·PbSO4·H2O)可用作聚氯乙烯的热稳定剂,200℃以上开始失去结晶水,不溶于水及有机溶剂。以200.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示。
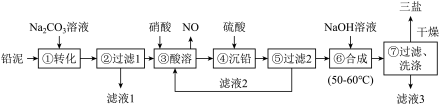
已知:PbSO4和PbCO3的溶解度和溶度积Ksp如下表。
(1)步骤①转化的目的是_______ ,滤液1中的溶质为Na2CO3和_______ (填化学式)。
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是_________ (任写一条)。其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为__________________ 。
(3)滤液2中可循环利用的溶质的化学式为_______ 。若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol/L,则此时c(SO42-)=______ mol/L。
(4)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是________________ 。
(5)步骤⑥合成三盐的化学方程式为____________ ,若得到纯净干燥的三盐99.Ot,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为________ 。

已知:PbSO4和PbCO3的溶解度和溶度积Ksp如下表。
| 化合物 | PbSO4 | PbCO3 |
| 溶解度/g | 1.03×10-4 | 1.81×10-7 |
| Ksp | 1.82×10-8 | 1.46×10-13 |
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是
(3)滤液2中可循环利用的溶质的化学式为
(4)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是
(5)步骤⑥合成三盐的化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



