解答题-实验探究题 较难0.4 引用2 组卷176
某工厂对工业污泥中的Cr元素回收与再利用的工艺如下(已知硫酸浸取液中的金属离子主要是Cr3+,其次是少量的Fe2+、Fe3+、Al3+、Ca2+、Mg2+):
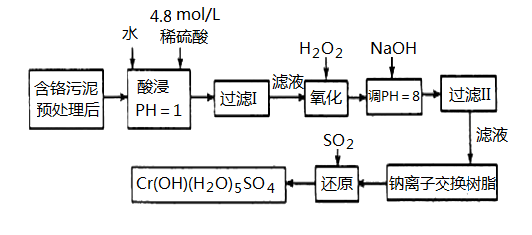
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
(1)实验室用98% (密度为1.84 g·cm-3)的浓硫酸配制200mL4.8 mol·L-1的硫酸溶液,配制时需要量取98%的浓硫酸的体积为_________ mL (保留小数点后一位小数),所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外,还需_____________________ 。
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏大的操作是___________ (填序号)
a.转移溶液时,没有等溶液冷却至室温b.量取浓硫酸时,俯视刻度线
c.当容量瓶中液体占容积2/3左右时,未振荡摇匀d.定容时俯视刻度线
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42-或Cr2O72-),以便于与杂质离子分离;另一方面是_____________________________ 。(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是___________________ 。
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是________________ 。
(6)通SO2气体时,其化学方程式为_______________________ 。

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | — | 一 | — |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 9 (>9溶解) |
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏大的操作是
a.转移溶液时,没有等溶液冷却至室温b.量取浓硫酸时,俯视刻度线
c.当容量瓶中液体占容积2/3左右时,未振荡摇匀d.定容时俯视刻度线
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42-或Cr2O72-),以便于与杂质离子分离;另一方面是
(4)调节溶液的pH=8除去的杂质离子是
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是
(6)通SO2气体时,其化学方程式为
17-18高三上·江西宜春·阶段练习
知识点:氧化还原反应方程式的配平配制一定物质的量浓度的溶液实验的误差分析配制一定物质的量浓度的溶液实验的仪器配制一定物质的量浓度溶液的综合考查 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
某工厂“对制革工业污泥中Cr(III)回收与再利用工艺如图(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
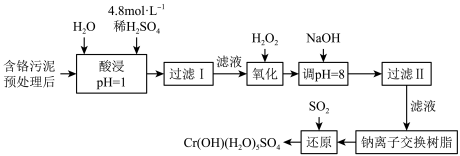
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
(1)实验室用18.4mol∙L-1的浓硫酸配制250mL4.8mol∙L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和移液管(一种能精确量取一定体积液体的仪器)外,还需___________ 。
(2)酸浸时,为了提高浸取率可采取的措施是___________ (至少两条)。
(3)加入H2O2的作用是___________ ,反应的离子方程式为___________
(4)钠离子交换树脂的原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是___________ 。
(5)还原过程发生以下反应(请完成):___________ 。
_______Na2Cr2O7+SO2+( )=_______Cr(OH)(H2O)5SO4+_______Na2SO4
(6)从流程的滤液中可回收的主要物质是___________

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ | Ca2+ |
| 开始沉淀时pH | 1.9 | 7.0 | ___ | __ | 4.7 | __ | ___ |
| 完全沉淀时pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) | 12.3 |
(1)实验室用18.4mol∙L-1的浓硫酸配制250mL4.8mol∙L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和移液管(一种能精确量取一定体积液体的仪器)外,还需
(2)酸浸时,为了提高浸取率可采取的措施是
(3)加入H2O2的作用是
(4)钠离子交换树脂的原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是
(5)还原过程发生以下反应(请完成):
_______Na2Cr2O7+SO2+( )=_______Cr(OH)(H2O)5SO4+_______Na2SO4
(6)从流程的滤液中可回收的主要物质是
某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
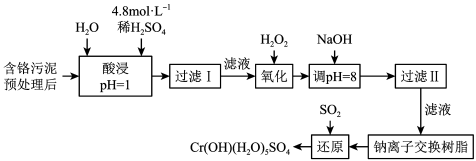
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
(1)实验室用18.4mol⋅L-1的浓硫酸配制250mL4.8mol⋅L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和移液管(一种能精确量取一定体积液体的仪器)外,还需___ 。
(2)酸浸时,为了提高浸取率可采取的措施是___ (至少两条)。
(3)加入H2O2的作用是___ 。
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是___ 。
(5)还原过程发生以下反应(请配平):__ Na2Cr2O7+__ SO2+__ =__ Cr(OH)(H2O)5SO4+__ Na2SO4;
(6)从流程的滤液中可回收的主要物质是___ 。

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解 |
(1)实验室用18.4mol⋅L-1的浓硫酸配制250mL4.8mol⋅L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和移液管(一种能精确量取一定体积液体的仪器)外,还需
(2)酸浸时,为了提高浸取率可采取的措施是
(3)加入H2O2的作用是
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是
(5)还原过程发生以下反应(请配平):
(6)从流程的滤液中可回收的主要物质是
利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下图所示:
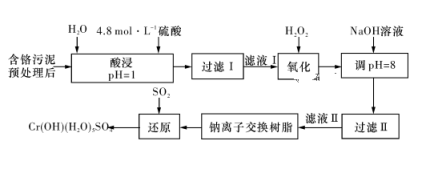
其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)实验室用18.4 mol·L-1的浓硫酸配制240 mL 4.8 mol·L-1的硫酸溶液,需量取浓硫酸__________ mL;配制时所用玻璃仪器除量筒、烧杯、胶头滴管和玻璃棒外,还需____________ 。
(2)“酸浸”时,为了提高浸取率可采取的措施有__________________ 。
(3)H2O2的作用是将“滤液Ⅰ”中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:___________________ 。
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。过滤后“滤液Ⅱ”中的阳离子主要有Na+、Ca2+、Mg2+,但溶液的pH不能超过8,其理由是__________________ 。
(5)钠离子交换树脂的反应原理为Mn++nNaR===MRn+nNa+,利用钠离子交换树脂除去“滤液Ⅱ”中的金属阳离子是________ (填离子符号)。
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:___________________ 。

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)实验室用18.4 mol·L-1的浓硫酸配制240 mL 4.8 mol·L-1的硫酸溶液,需量取浓硫酸
(2)“酸浸”时,为了提高浸取率可采取的措施有
(3)H2O2的作用是将“滤液Ⅰ”中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | — | — | — |
| 沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。过滤后“滤液Ⅱ”中的阳离子主要有Na+、Ca2+、Mg2+,但溶液的pH不能超过8,其理由是
(5)钠离子交换树脂的反应原理为Mn++nNaR===MRn+nNa+,利用钠离子交换树脂除去“滤液Ⅱ”中的金属阳离子是
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


