解答题-原理综合题 适中0.65 引用1 组卷663
(1)卫星发射时可用肼(N2H4)作燃料,8gN2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出155.5 kJ热量,写出反应的热化学方程式
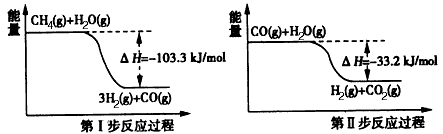
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H=-159.5 kJ/mol
②NH2CO2NH4(s)= CO(NH2)2(s) +H2O(g) △H=+116.5 kJ/mol
③H2O(l)=H2O(g) △H=+44 kJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式
(3)断裂1 mol化学键所需的能量如表所示:
| 共价键 | H—N | H—O | N≡N | O==O |
| 断裂1 mol化学键所需能量/kJ | 393 | 463 | 941 | 496 |
(4)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极在碱性条件下发生反应的电极反应式为
17-18高二上·福建泉州·阶段练习
类题推荐
目前我国主要使用肼(N2H4)作为卫星发射所用燃料。
(1)N2H4可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和H2O。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.2kJ·mol-1
写出液体燃料N2H4与液态N2O4反应的热化学方程式:_______________________________ 。
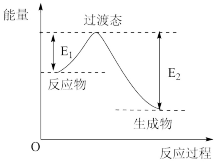
(2)在230℃和催化剂存在的条件下,将CO2与H2转化为CH3OH(g)和H2O(g)。如图为生产1 mol CH3OH(g)的能量变化示意图:
下表为破坏1 mol不同共价键所需的能量(kJ)。试计算:
①当CO2与H2转化为1 mol CH3OH(g)和H2O(g)的ΔH=_____________ 。
②已知E1=8.2kJ·mol-1,则E2=_________ kJ·mol-1。
(3)以H2合成尿素CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1
2NH3(g) ΔH=-92.4kJ·mol-1
②NH3(g)+ CO2(g)=
CO2(g)= NH2CO2NH4(s) ΔH=-79.7kJ·mol-1
NH2CO2NH4(s) ΔH=-79.7kJ·mol-1
③NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) ΔH=+72.5kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为_________ 。
(1)N2H4可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和H2O。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH=-19.5kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=-534.2kJ·mol-1
写出液体燃料N2H4与液态N2O4反应的热化学方程式:
(2)在230℃和催化剂存在的条件下,将CO2与H2转化为CH3OH(g)和H2O(g)。如图为生产1 mol CH3OH(g)的能量变化示意图:

下表为破坏1 mol不同共价键所需的能量(kJ)。试计算:
| C-H | C-O | C=O | H-H | H-O |
| 413.4 | 351 | 745 | 436 | 462.8 |
①当CO2与H2转化为1 mol CH3OH(g)和H2O(g)的ΔH=
②已知E1=8.2kJ·mol-1,则E2=
(3)以H2合成尿素CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)
②NH3(g)+
③NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) ΔH=+72.5kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网