解答题-原理综合题 适中0.65 引用1 组卷153
某消毒液的主要成分为 NaClO(混有少量NaCl)。
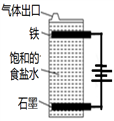
(1)该消毒液电解饱和的食盐水的方法制备,装置如图。写出该方法的总反应方程式:____________________ 。
(2)该消毒液中通入SO2气体时发生反应的离子方程式为:__________________ 。
(3)向盐酸酸化的FeCl2溶液中滴入少量该溶液,溶液颜色变成棕黄色,反应的离子方程式为_____________________ 。
(4)该消毒液做家用漂白精时,只要将该溶液露至在空气中就可以达到漂白效果。
(已知H2CO3的Ka1、Ka2与HClO的Ka关系为Ka1>Ka>Ka2)
用离子方程式解释其漂白原理___________________________ 。
(5)解释该消毒液不能与洁厕灵(主要成分为浓盐酸)混用的原因:_______________ 。
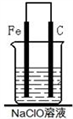
(6)为探究将一颗普通铁钉(含碳)放入该消毒液中发生腐蚀的原理,现设计如图实验装置,试写出碳电极上发生的电极反应式:______________________ 。
(1)该消毒液电解饱和的食盐水的方法制备,装置如图。写出该方法的总反应方程式:

(2)该消毒液中通入SO2气体时发生反应的离子方程式为:
(3)向盐酸酸化的FeCl2溶液中滴入少量该溶液,溶液颜色变成棕黄色,反应的离子方程式为
(4)该消毒液做家用漂白精时,只要将该溶液露至在空气中就可以达到漂白效果。
(已知H2CO3的Ka1、Ka2与HClO的Ka关系为Ka1>Ka>Ka2)
用离子方程式解释其漂白原理
(5)解释该消毒液不能与洁厕灵(主要成分为浓盐酸)混用的原因:
(6)为探究将一颗普通铁钉(含碳)放入该消毒液中发生腐蚀的原理,现设计如图实验装置,试写出碳电极上发生的电极反应式:

16-17高三·湖北荆州·阶段练习
类题推荐
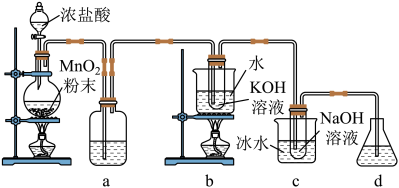
氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置 部分装置省略
部分装置省略 制备
制备 和
和 ,探究其氧化还原性质。
,探究其氧化还原性质。
(1)盛放 粉末的仪器名称是
粉末的仪器名称是_______ ,d装置的作用_______ 。
(2) 中的试剂为饱和食盐水,其作用是
中的试剂为饱和食盐水,其作用是_______ 和降低氯气的溶解度,请根据平衡移动的原理来解释氯气在饱和食盐水中溶解度低的原因:_______ 。
(3) 中化学反应的离子方程式是
中化学反应的离子方程式是_______ , 中化学反应的离子方程式是
中化学反应的离子方程式是_______ 。
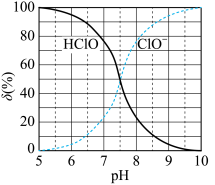
(4)生成的 具有漂白性,氯水中含有的HClO也具有漂白性。次氯酸为一元弱酸,其电离平衡体系中各成分的组成分数δ[δ(X)=
具有漂白性,氯水中含有的HClO也具有漂白性。次氯酸为一元弱酸,其电离平衡体系中各成分的组成分数δ[δ(X)= ,X为HClO或ClO−]与pH的关系如图所示。HClO的电离常数Ka值为
,X为HClO或ClO−]与pH的关系如图所示。HClO的电离常数Ka值为_______ 。又知某温度下碳酸的电离平衡常数如下:
写出少量的CO2通入84消毒液中的离子方程式:_______ 。
(1)盛放
(2)
(3)
(4)生成的
化学式 | H2CO3 |
电离平衡常数 | K1= 4.3×10-6 K2= 4.7×10-11 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


