解答题-实验探究题 较难0.4 引用5 组卷512
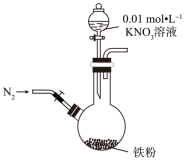
某同学看到“利用零价铁还原NO3-脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与KNO3溶液的反应。实验步骤及现象如下:

(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是______________________________ 。
(2)白色物质是__________ ,用化学方程式解释其变为红褐色的原因:____________________ 。
(3)为了探究滤液的成分,该同学进一步设计了下述实验:
(i)根据以上实验现象,可以判断滤液中存在____________________ 离子。
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因____________________ 。

| 实验步骤 | 实验现象 |
| 1、打开弹簧夹,缓慢通入N2 | |
| 2、加入pH为2.5的0.01mol/L酸性KNO3溶液100mL | 铁粉部分溶解,溶液呈浅绿色; 铁粉不再溶解后,剩余铁粉表面出现少量白色物质附着。 |
| 3、反应停止后,拔掉橡胶塞,将圆底烧瓶取下 | 烧瓶内气体的颜色没有发生变化。 |
| 4、将剩余固体过滤 | 表面的白色物质变为红褐色。 |
(2)白色物质是
(3)为了探究滤液的成分,该同学进一步设计了下述实验:
| 实验步骤 | 实验现象 |
| 1、取部分滤液于试管中,向其中加入KSCN溶液 | 溶液液无变化 |
| 2、将上述溶液分为两份,一份中滴入氯气;另一份中滴加稀硫酸 | 两份溶液均变为红色 |
| 3、另取部分滤液于试管中,向其中加入浓NaOH溶液并加热,在试管口放置湿润的红色石蕊试纸。 | 有气体生成,该气体使红色石蕊试纸变蓝。 |
(ii)步骤2中滴加稀硫酸后溶液会由浅绿色变成红色,请用离子方程式解释其原因
15-16高一下·北京·期末
类题推荐
某同学看到“利用零价铁还原 脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与
脱除地下水中硝酸盐”的相关资料后,利用如下装置探究铁粉与 溶液的反应。实验过程如下:
溶液的反应。实验过程如下:

i.打开弹簧夹,缓慢通入 ,并保持后续反应均在
,并保持后续反应均在 氛围中进行;
氛围中进行;
ii.加入pH 已调至2.5 的
 酸性溶液100mL,一段时间后铁粉部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;
酸性溶液100mL,一段时间后铁粉部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;
iii.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在 、
、 和
和 。
。
(1)通入 并保持后续反应均在
并保持后续反应均在 氛围中进行的实验目的是
氛围中进行的实验目的是_________ 。
(2)白色物质是_________ ,用化学方程式解释其变为红褐色的原因:_________ 。
(3)用 检验滤液中
检验滤液中 的实验方案是
的实验方案是_________ 。
(4)取少量滤液,向其中加入几滴KSCN 溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色。溶液变成红色的原因是_________ 。
(5)该同学进一步查阅资料发现,用铁粉、碳粉的混合物脱除硝酸盐,效果更佳。他用上述 溶液继续设计如下实验,探究碳粉的作用。
溶液继续设计如下实验,探究碳粉的作用。
实验操作①处填:_______ ,现象及结论②处填________ 。
关于碳粉的作用,还可以提出的假设是_______ 。

i.打开弹簧夹,缓慢通入
ii.加入pH 已调至2.5 的
iii.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在
(1)通入
(2)白色物质是
(3)用
(4)取少量滤液,向其中加入几滴KSCN 溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色。溶液变成红色的原因是
(5)该同学进一步查阅资料发现,用铁粉、碳粉的混合物脱除硝酸盐,效果更佳。他用上述
| 假设 | 实验操作 | 现象及结论 |
| 假设1:碳粉可用作还原 剂,脱除硝酸盐 | 向烧杯中加入___①____,一段 时间后,测定烧杯中 浓度 | 明假设1不成立 |
| 假设2:碳粉、铁粉形成 无数个微小的原电池,促 进了硝酸盐的脱除 | 按下图所示组装实验装置,一 段时间后,测定  | ____②____,说明假设2 成立 |
关于碳粉的作用,还可以提出的假设是
某同学看到利用零价铁还原NO3-脱除地下水中硝酸盐”的相关报道后,利用如下装置探究铁粉与KNO3溶液的反应。实验过程如下:

ⅰ.打开弹簧夹,缓慢通入N2,并保持后续反应均在N2氛围中进行;
ii.加入pH已调至2.5的0.01mol·L-1KNO3酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;
ⅲ.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在NO3-、NH4+和Fe2+。
(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是______________________ 。
(2)用化学方程式解释其变为红褐色的原因:_________________________________ 。
(3)用K3[Fe(CN)6]检验滤液中Fe2+的实验方案是(写出具体操作、现象及结论)___________ 。
(4)取少量滤液,向其中加入几滴KSCN溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色。溶液变成红色的原因是_________________________________ 。
(5)该同学进一步查阅文献发现,用铁粉、碳粉混合物脱除硝酸盐,效果更佳。他用上述KNO3溶液继续设计如下实验,探究碳粉的作用。
③关于碳粉的作用,还可以提出的合理假设是_________________________________ 。

ⅰ.打开弹簧夹,缓慢通入N2,并保持后续反应均在N2氛围中进行;
ii.加入pH已调至2.5的0.01mol·L-1KNO3酸性溶液100mL,一段时间后铁屑部分溶解,溶液逐渐变为浅绿色;待铁粉不再溶解,静置后发现,剩余固体表面有少量白色物质附着;
ⅲ.过滤剩余固体时,表面的白色物质变为红褐色;
iv.检测到滤液中存在NO3-、NH4+和Fe2+。
(1)通入N2并保持后续反应均在N2氛围中进行的实验目的是
(2)用化学方程式解释其变为红褐色的原因:
(3)用K3[Fe(CN)6]检验滤液中Fe2+的实验方案是(写出具体操作、现象及结论)
(4)取少量滤液,向其中加入几滴KSCN溶液,无明显现象;再加入几滴稀硫酸,溶液呈红色。溶液变成红色的原因是
(5)该同学进一步查阅文献发现,用铁粉、碳粉混合物脱除硝酸盐,效果更佳。他用上述KNO3溶液继续设计如下实验,探究碳粉的作用。
| 假设 | 实验操作 | 现象及结论 |
| 假设1:碳粉可用作还原剂,脱除硝酸盐 | 向烧杯中加入① | NO3-浓度无明显变化,说明假设1不成立 |
| 假设2:碳粉、铁粉形成无数个微小的原电池,促进了硝酸盐的脱除 | 按如图所示组装实验装置,一段时间后,测定NO3-浓度 | ② |
③关于碳粉的作用,还可以提出的合理假设是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网