解答题-实验探究题 较难0.4 引用1 组卷275
草酸和高锰酸钾能发生反应: 2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
Ⅰ.某小组同学探究草酸浓度对反应速率的影响时,设计了如下系列实验:
(1)V1=___________ ; V2=___________ 。
(2)褪色时间t1、t2、t3由长到短的顺序为____________________ 。
Ⅱ.在探究浓度对速率的影响时,同学们发现溶液褪色先慢后快,即反应速率由小变大。大家对此“异常”现象展开了讨论,根据外界条件对速率的影响进行分析,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
(1)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是___________ 。
(2)猜想Ⅱ可能是______________________ 。要设计实验验证猜想Ⅱ,进行该实验还要补充的一种试剂是___________ 。
Ⅰ.某小组同学探究草酸浓度对反应速率的影响时,设计了如下系列实验:
| 实验序号 | KMnO4酸性洛液 | H2C2O4溶液 | H2O | 褪色时间 | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 10.0 | 0.01 | 5.0 | 0.50 | V1 | t1 |
| ② | 10.0 | 0.01 | V2 | 0.50 | 2.0 | t2 |
| ③ | 10.0 | 0.01 | 10.0 | 0.50 | 0 | t3 |
(2)褪色时间t1、t2、t3由长到短的顺序为
Ⅱ.在探究浓度对速率的影响时,同学们发现溶液褪色先慢后快,即反应速率由小变大。大家对此“异常”现象展开了讨论,根据外界条件对速率的影响进行分析,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
(1)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是
(2)猜想Ⅱ可能是
16-17高二下·广西桂林·期末
类题推荐
І.Na2S2O3用于照相业定影剂、鞣革时重铬酸盐的还原剂等。回答下列问题:
(1)Na2S2O3溶液与稀硫酸的反应可探究外界条件对化学反应速率的影响,Na2S2O3溶液与稀硫酸反应的化学方程式为_______ ;
(2)某同学探究影响硫代硫酸钠溶液与稀硫酸反应速率的因素时,设计如下系列实验:
回答下列问题:该实验①、②可探究_______ 对反应速率的影响,因此V3=_______ ;实验①、③可探究_______ 对反应速率的影响,因此V5=_______ 。
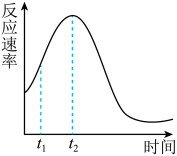
Ⅱ.某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时(2KMnO4+5H2C2O4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O),发现反应速率变化如图所示,小组成员探究t1~ t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种。
猜想I:此反应过程放热,温度升高,反应速率加快:
猜想II:……
(3)猜想II可能是:_______ 。
(4)基于猜想II成立,设计方案进行实验,请完成以下实验记录表内容。
(1)Na2S2O3溶液与稀硫酸的反应可探究外界条件对化学反应速率的影响,Na2S2O3溶液与稀硫酸反应的化学方程式为
(2)某同学探究影响硫代硫酸钠溶液与稀硫酸反应速率的因素时,设计如下系列实验:
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
Ⅱ.某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时(2KMnO4+5H2C2O4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O),发现反应速率变化如图所示,小组成员探究t1~ t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种。

猜想I:此反应过程放热,温度升高,反应速率加快:
猜想II:……
(3)猜想II可能是:
(4)基于猜想II成立,设计方案进行实验,请完成以下实验记录表内容。
| 加入试剂 | 2mL 0.1mol/LH2C2O4溶液、1mL0.05mol/L酸性KMnO4 | 2mL 0.1mol/LH2C2O4溶液、1mL0.05mol/L酸性KMnO4,少量 |
| 实验现象 | 褪色时间10min | 褪色时间 |
| 结论 | 猜想II正确 | |
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”,进行了如下实验:2KMnO4+5H2C2O4 +3H2SO4 =2MnSO4 +K2SO4 +10CO2↑ +8H2O
请回答:
(1)实验计时方法是从溶液混合开始记时,至____ 时记时结束;
(2)V1=___ ,V2=___ ;设计实验Ⅰ、Ⅲ的目的是______ ;
(3)利用实验Ⅲ中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=___ ;
(4)有同学在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。某同学认为是放热导致溶液温度升高所致,重做Ⅰ号实验,测定过程中溶液不同时间的温度,结果温度没有明显变化。由此你得出的结论是:
①____ 不是反应速率突然加快的原因;
②可能是反应产物有催化作用。Ⅳ号实验是为验证你的猜测,实验中要加入的少量某种物质是____ (填化学式)
| 编号 | 0.01mol•L-1 酸性KMnO4溶液 | 0.1mol•L-1 H2C2O4溶液 | 水 | 某种物质 | 反应温度/℃ | 反应时间 (min) |
| Ⅰ | 2mL | 2mL | 0 | 0 | 20 | 2.1 |
| Ⅱ | V1mL | 2mL | 1mL | 0 | 20 | 5.5 |
| Ⅲ | V2 mL | 2mL | 0 | 0 | 50 | 0.5 |
| Ⅳ | 2mL | 2mL | 0 | 少量 | 20 | 0.2 |
(1)实验计时方法是从溶液混合开始记时,至
(2)V1=
(3)利用实验Ⅲ中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=
(4)有同学在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。某同学认为是放热导致溶液温度升高所致,重做Ⅰ号实验,测定过程中溶液不同时间的温度,结果温度没有明显变化。由此你得出的结论是:
①
②可能是反应产物有催化作用。Ⅳ号实验是为验证你的猜测,实验中要加入的少量某种物质是
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”,进行了如下实验:
请回答:
(1)已知KMnO4酸性溶液与H2C2O4溶液反应有CO2生成,用化学方程式表示该实验的实验原理:__________________________________________________________________ 。
(2)实验计时方法是从溶液混合开始记时,至_________________ 时记时结束。
(3)V1=_____ ,V2=_____ ;设计实验Ⅰ、Ⅲ的目的是______________________________ 。
(4)利用实验Ⅲ中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=________ 。
(5)有同学在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。某同学认为是放热导致溶液温度升高所致,重做Ⅰ号实验,测定过程中溶液不同时间的温度,结果温度没有明显变化。由此你得出的结论是:
①________ 不是反应速率突然加快的原因;
②可能是反应产物有催化作用。Ⅳ号实验是为验证你的猜测,实验中要加入的少量某种物质是___________ 。
| 实验编号 | 0.01mol•L﹣1 酸性KMnO4溶液 | 0.1mol•L﹣1 H2C2O4溶液 | 水 | 某种物质 | 反应温度/℃ | 反应时间(min) |
| Ⅰ | 2ml | 2ml | 0 | 0 | 20 | 2.1 |
| Ⅱ | V1ml | 2ml | 1ml | 0 | 20 | 5.5 |
| Ⅲ | V2 ml | 2ml | 0 | 0 | 50 | 0.5 |
| Ⅳ | 2ml | 2ml | 0 | 少量 | 20 | 0.2 |
(1)已知KMnO4酸性溶液与H2C2O4溶液反应有CO2生成,用化学方程式表示该实验的实验原理:
(2)实验计时方法是从溶液混合开始记时,至
(3)V1=
(4)利用实验Ⅲ中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=
(5)有同学在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。某同学认为是放热导致溶液温度升高所致,重做Ⅰ号实验,测定过程中溶液不同时间的温度,结果温度没有明显变化。由此你得出的结论是:
①
②可能是反应产物有催化作用。Ⅳ号实验是为验证你的猜测,实验中要加入的少量某种物质是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


