单选题 适中0.65 引用1 组卷197
已知:①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220kJ·mol-1
②断裂1 mol H2(g)中的H—H键需要吸收436 kJ的能量,断裂1mol O2(g)中的共价键需要吸收496kJ的能量,生成H2O(g)中的1 mol H—O键能放出462 kJ的能量。则下列说法正确的是
2C(s)+O2(g)=2CO(g) ΔH2=-220kJ·mol-1
②断裂1 mol H2(g)中的H—H键需要吸收436 kJ的能量,断裂1mol O2(g)中的共价键需要吸收496kJ的能量,生成H2O(g)中的1 mol H—O键能放出462 kJ的能量。则下列说法正确的是
| A.断裂1 mol H2O(l)中化学键形成H、O原子的过程中需吸收的能量为924 kJ |
| B.a的值为-130 |
| C.2H2(g)+O2(g)=2H2O(g) ΔH =-(220+2a)kJ·mol-1 |
| D.加入某一催化剂能同等程度降低ΔH1、ΔH2的大小 |
16-17高二下·浙江嘉兴·期末
类题推荐
已知断裂1mol H2(g)中的H—H键需要吸收436.4kJ的能量,断裂1molO2(g)中的共价键需要吸收498kJ的能量,生成H2O(g)中的1mol H—O键能放出462.8kJ的能量。下列说法正确的是
| A.断裂1mol H2O中的化学键需要吸收925.6kJ的能量 |
| B.2H2(g)+ O2(g)=2H2O (g) △H=-480.4 kJ·mol-1 |
| C.2H2O(l) = 2H2 (g) + O2(g) △H=-471.6 kJ·mol-1 |
| D.H2(g)+ 1/2O2(g)=H2O (l) △H=-240.2 kJ·mol-1 |
已知断裂1 mol H2(g)中的H-H键需要吸收436.4 kJ的能量,断裂1 mol O2(g)中的共价键需要吸收498 kJ的能量,生成H2O(g)中的1 mol H-O键能放出462.8 kJ的能量。下列说法正确的是
| A.断裂1 mol H2O中的化学键需要吸收925.6 kJ的能量 |
| B.H2(g)+ |
| C.2H2O(l)=2H2(g)+O2(g) ΔH=471.6 kJ·mol-1 |
| D.H2(g)+ |
如图所示a=1 370.8,b=1 851.2。下列说法不正确的是
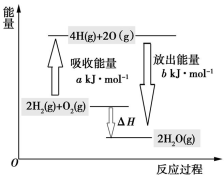

| A.由H(g)和O(g)形成1 mol H—O键,放出462.8 kJ的能量 |
B.图示热化学方程式可表示为:2H2(g)+O2(g) 2H2O(l) ΔH=-480.4 kJ·mol-1 2H2O(l) ΔH=-480.4 kJ·mol-1 |
| C.如果断裂1 mol H2(g)中的H—H键需要吸收436.4 kJ的能量,则断裂1 mol O2(g)中的共价键需要吸收498 kJ的能量 |
D.2H2O(g) 2H2(g)+O2(g) ΔH=+480.4 kJ·mol-1 2H2(g)+O2(g) ΔH=+480.4 kJ·mol-1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


