解答题-工业流程题 较难0.4 引用2 组卷166
电镀污泥是指电镀废水处理后产生的污泥和镀槽淤泥,被列入国家危险废物名录,属于第十七类危险废物。电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧—钠氧化法”回收得到Na2Cr2O7等物质。
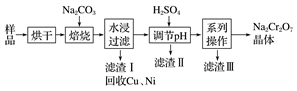
已知:①水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质
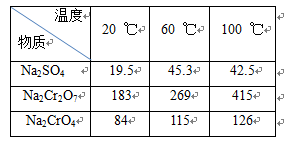
②不同钠盐在不同温度下的溶解度(g)如下表
(1)水浸后的溶液呈________ (“酸”“碱”或“中”)性。
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式:
______________________________
(3)滤渣Ⅱ的主要成分有Zn(OH)2、________ 。
(4)“系列操作”中为继续加入H2SO4,________________ (填操作方法),过滤。继续加入H2SO4目的是_____________________ (结合平衡移动的原理予 以说明)。
以说明)。
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨作电极电解生产金属铬,写出生成铬的电极反应方程式:________________________________________________ 。

已知:①水浸后溶液中存在Na2CrO4、NaAlO2、Na2ZnO2等物质
②不同钠盐在不同温度下的溶解度(g)如下表

(1)水浸后的溶液呈
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式:
(3)滤渣Ⅱ的主要成分有Zn(OH)2、
(4)“系列操作”中为继续加入H2SO4,
 以说明)。
以说明)。(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨作电极电解生产金属铬,写出生成铬的电极反应方程式:
2017高三上·浙江·专题练习
类题推荐
工业上“中温焙烧——钠化氧化法”回收电镀污泥中的铬已获技术上的突破。其工艺流程如下:
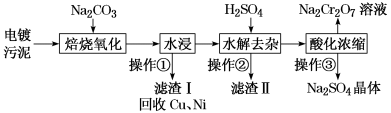
[查阅资料]①电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质
②Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
请回答:
(1)操作①的名称是___________ , “水浸”后的溶液呈___________ 性
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为___________ 。
(3)滤渣Ⅱ的主要成分有Zn(OH)2和X,生成X的离子反应方程式为___________
(4)“酸化浓缩”时,需继续加入H2SO4,使Na2CrO4转化成Na2Cr2O7,反应的离子方程式为___________

[查阅资料]①电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质
②Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
温度 化学式 | 20 ℃ | 60 ℃ | 100 ℃ |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
| Na2CrO4 | 84 | 115 | 126 |
(1)操作①的名称是
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为
(3)滤渣Ⅱ的主要成分有Zn(OH)2和X,生成X的离子反应方程式为
(4)“酸化浓缩”时,需继续加入H2SO4,使Na2CrO4转化成Na2Cr2O7,反应的离子方程式为
工业上“中温焙烧——钠化氧化法”回收电镀污泥中的铬已获技术上的突破。其工艺流程如下:
【查阅资料】
①电镀污泥中含有Cr(OH)3、Al203、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质;
②Na2CrO4转化成Na2Cr2O7离子反应方程式为:2 CrO42-+2H+=Cr2O72-+H2O;③Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
请回答:
(1)操作①的名称是_______ ,“水浸”后的溶液呈_______ 性;
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为___________ ;
(3)滤渣II的主要成分有Zn(OH)2和X,生成X的离子反应方程式__________ ;
(4)“酸化浓缩”时,需继续加入H2SO4,然后_______ 、结晶、过滤。继续加入H2SO4目的是__________ ;
(5)以铬酸钠为原料,电化学法制备重铬酸钠的实验装置如图所示。
①阴极发生的电极反应式为:_____________ ;
②若测定阳极液中Na与Cr的物质的量之比值为d,则此时铬酸钠的转化率为___________ 。

【查阅资料】
①电镀污泥中含有Cr(OH)3、Al203、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质;
②Na2CrO4转化成Na2Cr2O7离子反应方程式为:2 CrO42-+2H+=Cr2O72-+H2O;③Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:
| 20℃ | 60℃ | 100℃ |
Na2SO4 | 19.5 | 45.3 | 42.5 |
Na2Cr2O7 | 183 | 269 | 415 |
Na2CrO4 | 84 | 115 | 126 |
请回答:
(1)操作①的名称是
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为
(3)滤渣II的主要成分有Zn(OH)2和X,生成X的离子反应方程式
(4)“酸化浓缩”时,需继续加入H2SO4,然后
(5)以铬酸钠为原料,电化学法制备重铬酸钠的实验装置如图所示。

①阴极发生的电极反应式为:
②若测定阳极液中Na与Cr的物质的量之比值为d,则此时铬酸钠的转化率为
电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过下述流程回收Na2Cr2O7等物质。
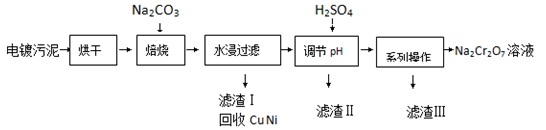
已知:
①Cr(OH)3、ZnO和Al2O3一样均为两性化合物;
②Na2Cr2O7、Na2SO4在不同温度下的溶解度如下表:
(1)焙烧过程中生成Na2CrO4的化学方程式为_______________ ;水浸后溶液中除Na2CrO4还存在的溶质有_______________ 和_______________ ;
(2)加入H2SO4调节pH的目的为____________________________ ;
(3)得到滤渣Ⅲ的“系列操作”的步骤为______________ 、______________ 过滤;
(4)若1L加入H2SO4后所得溶液中含铬元素质量为23.4g,CrO42﹣有8/9转化为Cr2O72﹣,求转化后所得溶液中c(Cr2O72﹣) =_________ mol•L﹣1;
(5)向Na2Cr2O7与H2SO4混合液中加入H2O2,再加入乙醚并摇动,乙醚层为蓝色。乙醚中溶有CrO5,则发生反应的化学方程式为_________________________ 。

已知:
①Cr(OH)3、ZnO和Al2O3一样均为两性化合物;
②Na2Cr2O7、Na2SO4在不同温度下的溶解度如下表:
| 20℃ | 60℃ | 100℃ | |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
(2)加入H2SO4调节pH的目的为
(3)得到滤渣Ⅲ的“系列操作”的步骤为
(4)若1L加入H2SO4后所得溶液中含铬元素质量为23.4g,CrO42﹣有8/9转化为Cr2O72﹣,求转化后所得溶液中c(Cr2O72﹣) =
(5)向Na2Cr2O7与H2SO4混合液中加入H2O2,再加入乙醚并摇动,乙醚层为蓝色。乙醚中溶有CrO5,则发生反应的化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



