解答题-原理综合题 适中0.65 引用1 组卷116
消除氮氧化物、二氧化硫等物质造成的污染是目前研究的重要课题。
(1)燃煤烟气脱硫常用如下方法。
①用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:2CO(g)+SO2(g)=S(g)+2CO2(g) △H1= + 8.0 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJ·mol-1
则H2(g)还原SO2(g)生成S(g)和H2O(g)的热化学方程式为______________________ 。
②一氧化碳还原法:在绝热恒容的密闭容器中,反应2CO(g)+SO2(g) S(s)+2CO2(g)达到平衡时,下列说法正确的是
S(s)+2CO2(g)达到平衡时,下列说法正确的是____ (填序号)。
a.容器内气体的压强保持不变 b.分离出S,正反应速率减小
若再充入一定量的CO2,反应的平衡常数不变
③用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。实验测得NH4HSO3溶液中 =15,则溶液的pH为
=15,则溶液的pH为________ 。 (已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)
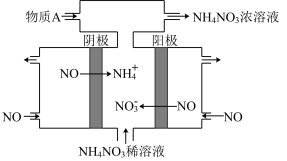
(2)电解NO可以制备NH4NO3,其工作原理如下图所示,阳极的电极反应式为:____________ ,为使电解产物全部转化为NH4NO3,需补充物质A,A是___________ 。
(3)Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+,滴加Na2S溶液后首先析出的沉淀是________ 。当最后一种离子沉淀完全时(该离子浓度为10-5 mol·L-1),此时S2-的浓度为_________________________
(已知: Ksp(FeS)=6.3×10-18 ;Ksp(CuS)=6×10-36 ;Ksp(PbS)=2.4×10-28)
(1)燃煤烟气脱硫常用如下方法。
①用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:2CO(g)+SO2(g)=S(g)+2CO2(g) △H1= + 8.0 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJ·mol-1
则H2(g)还原SO2(g)生成S(g)和H2O(g)的热化学方程式为
②一氧化碳还原法:在绝热恒容的密闭容器中,反应2CO(g)+SO2(g)
 S(s)+2CO2(g)达到平衡时,下列说法正确的是
S(s)+2CO2(g)达到平衡时,下列说法正确的是a.容器内气体的压强保持不变 b.分离出S,正反应速率减小
若再充入一定量的CO2,反应的平衡常数不变
③用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。实验测得NH4HSO3溶液中
(2)电解NO可以制备NH4NO3,其工作原理如下图所示,阳极的电极反应式为:

(3)Na2S是常用的沉淀剂。某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+,滴加Na2S溶液后首先析出的沉淀是
(已知: Ksp(FeS)=6.3×10-18 ;Ksp(CuS)=6×10-36 ;Ksp(PbS)=2.4×10-28)
16-17高二下·山东济宁·期末
类题推荐
消除氮氧化物、二氧化硫等物质造成的污染是目前研究的重要课题。
(1)工业上常用活性炭还原一氧化氮,其反应为:2NO(g)+C(s) N2(g)+CO2(g)。向容积均为lL的甲、乙、丙三个恒容恒温容器中分别加入足量的活性炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g)。向容积均为lL的甲、乙、丙三个恒容恒温容器中分别加入足量的活性炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
①甲容器反应温度T℃__ 400℃(填“>”或“<”或“=”);
②乙容器中,0~40min内平均反应速率v(N2)=__ ;
③丙容器中达平衡后NO的转化率为__ 。
(2)活性炭还原NO2的反应为:2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,lmolNO2和足量活性炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,lmolNO2和足量活性炭发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:

①A、B、C三点中NO2的转化率最高的是__ 点(填“A”或“B”或“C”)。
②计算C点时该反应的压强平衡常数KP=__ MPa(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)燃煤烟气脱硫常用如下方法。
方法①:用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:
2CO(g)+SO2(g)=S(g)+2CO2(g) △H1=8.0kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJ·mol-1
则H2(g)还原SO2(g)生成S(g)和H2O(g)的热化学方程式为__ 。
方法②:用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4,则用氨水将SO2转化为NH4HSO3的离子方程式为__ ;实验测得NH4HSO3溶液中 =15,则溶液的pH为
=15,则溶液的pH为__ 。(已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)
(1)工业上常用活性炭还原一氧化氮,其反应为:2NO(g)+C(s)
t/min n(NO)/mol T | 0 | 40 | 80 | 120 | 160 | |
| 甲 | T℃ | 2 | 1.45 | 1 | 1 | 1 |
| 乙 | 400℃ | 2 | 1.5 | 1.1 | 0.8 | 0.8 |
| 丙 | 400℃ | 1 | 0.8 | 0.65 | 0.53 | 0.45 |
①甲容器反应温度T℃
②乙容器中,0~40min内平均反应速率v(N2)=
③丙容器中达平衡后NO的转化率为
(2)活性炭还原NO2的反应为:2NO2(g)+2C(s)

①A、B、C三点中NO2的转化率最高的是
②计算C点时该反应的压强平衡常数KP=
(3)燃煤烟气脱硫常用如下方法。
方法①:用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:
2CO(g)+SO2(g)=S(g)+2CO2(g) △H1=8.0kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJ·mol-1
则H2(g)还原SO2(g)生成S(g)和H2O(g)的热化学方程式为
方法②:用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4,则用氨水将SO2转化为NH4HSO3的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


 H2S(g) +CO(g)
H2S(g) +CO(g)