单选题 适中0.65 引用1 组卷200
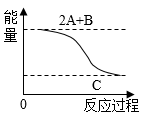
已知反应:2A+B = C在一定条件下进行的能量变化如图所示,破坏1mol A中的化学键消耗的能量为Q1 kJ,破坏1mol B中的化学键消耗的能量为Q2 kJ,形成1mol C中的化学键释放的能量为Q3 kJ.请判断以下说法正确的是

| A.该反应中存在以下关系:2 Q1+ Q2< Q3 |
| B.该反应的能量转化形式只能以热能的形式进行 |
| C.当有1molB参加反应时,该反应放出的热量为:Q3 kJ |
| D.此反应为放热反应,所以在常温下一定能发生 |
16-17高一下·福建龙岩·阶段练习
类题推荐
已知反应H2+Cl2=2HCl,破坏1molH2中的化学键消耗的能量为Q1kJ,破坏1molCl2中的化学键消耗的能量为Q2kJ,形成1molHCl中的化学键释放的能量为Q3kJ,则下列说法中正确的是
| A.该反应反应物的总能量高于生成物的总能量 |
| B.该反应的能量关系为Q1+Q2<Q3 |
| C.该反应需要在点燃或光照下进行,所以为吸热反应 |
| D.该反应中化学能只能转化为热能 |
已知反应A2+B2=2AB,破坏1 mol A2中的化学键消耗的能量为Q1 kJ,破坏1 mol B2中的化学键消耗的能量为 Q2 kJ,形成1 mol AB中的化学键释放的能量为Q3 kJ,则下列说法正确的是
| A.若A2和B2的总能量之和大于生成的AB的总能量,则反应放热 |
| B.若A2和B2的总能量之和小于生成的AB的总能量,则反应放热 |
| C.若该反应放出能量,则Q1+Q2>Q3 |
| D.若该反应吸收能量,则Q1+Q2<Q3 |
已知氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ,则下列关系式中一定正确的是
| A.Q1+Q2<2Q3 | B.Q1+Q2>2Q3 | C.Q1+Q2<Q3 | D.Q1+Q2=Q3 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


