解答题-结构与性质 适中0.65 引用1 组卷315
硒化锌是一种透明色半导体,也可作为红外光学材料,熔点是1 520 ℃。(1)基态锌原子的价电子排布式是________。(2)根据元素周期律,电负性Se________S,第一电离能Se________As(填“>”或“<”)。(3)H2S分子的电子式:________,H2Se分子构型是_______,其中硒原子的杂化轨道类型是________。(4)H2O的沸点高于H2Se的沸点(-42 ℃),其原因是________。(5)晶体Zn为六方最密堆积,其配位数是________。(6)ZnSe晶胞如图,假设阿伏伽德罗常数的值为NA,则144 g ZnSe晶体中的晶胞数是________。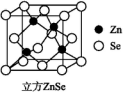
2017·广西桂林·一模
知识点:电子排布式电离能变化规律晶胞的有关计算 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录 类题推荐 Ⅰ. 硒化锌是一种透明半导体,也可作为红外光学材料,熔点是1 520 ℃。
(1)基态锌原子的价电子排布式是_______。
(2)根据元素周期律,电负性Se____S,第一电离能Se____As(填“>”或“<”)。
(3)H2Se的分子构型是____,其中硒原子的杂化轨道类型是____。
(4)H2O的沸点高于H2Se的沸点(-42 ℃),其原因是________________。
(5)晶体Zn为六方最密堆积,其配位数是____。
Ⅱ 氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)C、N、O三种元素第一电离能从大到小的顺序是________。
(2)1 mol N2F2含有____ mol σ键。
(3)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含____ mol配位键。
(4)安全气囊打开时发生的化学反应为10NaN3+2KNO3 = K2O+5Na2O+16N2↑。
①写出与N2互为等电子体的分子________。
②Na2O的晶胞结构如图所示,晶胞边长为566 pm,晶胞中氧原子的配位数为____,Na2O晶体的密度为______(只要求列算式,不必计算出结果),Na+与O2-间的最短距离为_____pm。

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

打开组卷App 获取专属积分,充值下载直接抵现