解答题-实验探究题 较难0.4 引用1 组卷522
(1)MgCl2·6H2O晶体受热水解可以生成MgOHCl,但产率较低,其化学方程式为_____________ 。
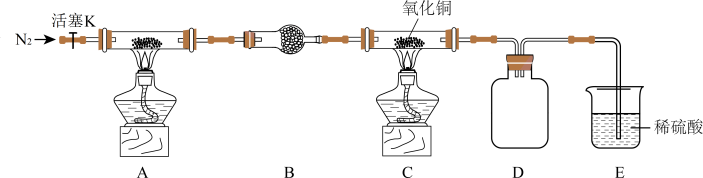
I.先用空气得到氮气,可供选择的装置和药品如图(还原铁粉已干燥,装置内发生的反应是完全的)。

(2)连接并检查装置的气密性。实验开始时,打开自来水的开关,将空气从5L的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)h→________________ 。
II.将得到的氮气通入如图装置参与制备碱式氯化镁并探究氨的催化氧化反应(其中CuO的质量为8.0g)。
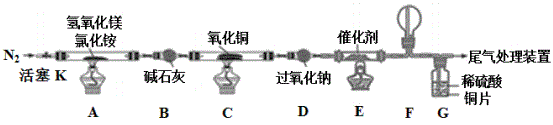
(3)装置A中发生反应生成碱式氯化镁的化学方程为_______________ 。
(4)实验结束时进行正确操作是________________ 。
A.关闭活塞K,先熄灭A处酒精灯,后熄灭C、E处酒精灯
B.先熄灭A处酒精灯,关闭活塞K,后熄灭C、E处酒精灯
C.先熄灭A处酒精灯,再熄灭C、E处酒精灯,后关闭活塞K
(5)反应完毕,装置C中的氧化铜完全反应,由黑色变为红色,甲同学设计一个实验方案,证明装置C中完全反应后的红色固体中含Cu2O。已知:①Cu2O+H+= Cu2++ Cu;②限选试剂:2 mol/L H2SO4溶液、12 mol/L H2SO4溶液、2 mol/L HNO3溶液、10 mol/L HNO3溶液。
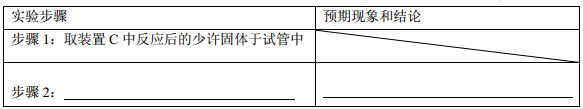
________ ,________ ,
乙同学称量C中红色物质,质量为6.8g,且生成的气体可直接排放到大气中,进一步确定红色固体是________ ,该反应中电子转移的物质的量为_________ mol。
I.先用空气得到氮气,可供选择的装置和药品如图(还原铁粉已干燥,装置内发生的反应是完全的)。

(2)连接并检查装置的气密性。实验开始时,打开自来水的开关,将空气从5L的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)h→
II.将得到的氮气通入如图装置参与制备碱式氯化镁并探究氨的催化氧化反应(其中CuO的质量为8.0g)。

(3)装置A中发生反应生成碱式氯化镁的化学方程为
(4)实验结束时进行正确操作是
A.关闭活塞K,先熄灭A处酒精灯,后熄灭C、E处酒精灯
B.先熄灭A处酒精灯,关闭活塞K,后熄灭C、E处酒精灯
C.先熄灭A处酒精灯,再熄灭C、E处酒精灯,后关闭活塞K
(5)反应完毕,装置C中的氧化铜完全反应,由黑色变为红色,甲同学设计一个实验方案,证明装置C中完全反应后的红色固体中含Cu2O。已知:①Cu2O+H+= Cu2++ Cu;②限选试剂:2 mol/L H2SO4溶液、12 mol/L H2SO4溶液、2 mol/L HNO3溶液、10 mol/L HNO3溶液。

乙同学称量C中红色物质,质量为6.8g,且生成的气体可直接排放到大气中,进一步确定红色固体是
2017·黑龙江哈尔滨·模拟预测
类题推荐
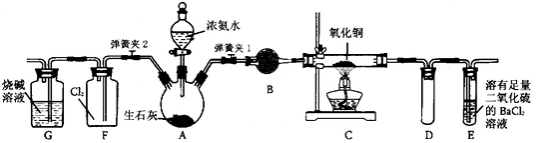
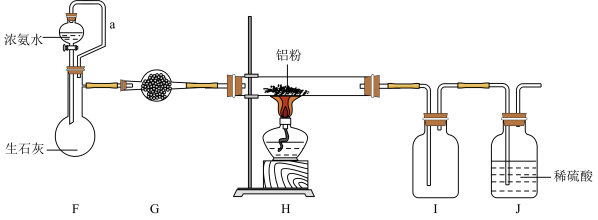
碱式氯化镁(MgOHCl)常用于塑料添加剂,工业上制备方法较多,其中利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁的工艺属于我国首创。某科研小组同学根据该原理设计了如图实验装置来制备碱式氯化镁并探究氨的催化氧化反应,其中CuO的质量为8.0g。
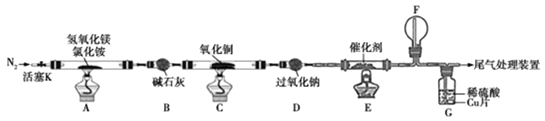
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为______________________。
(2)反应过程中持续通入N2的作用有两点:一是使装置A中产生的氨气完全导出,二是____________。
(3)一段时间后,你认为装置F中可观察到什么现象?_______________________。
(4)用离子方程式解释装置G中溶液变成蓝色的原因:_______________________。
(5)反应完毕,装置C中的氧化铜完全反应,由黑色变为红色,称其质量为6.8g,且生成的气体可直接排放到大气中,则红色固体是_______,该反应中电子转移的物质的量为__________mol。
(6)请你设计一个实验方案,证明装置C中完全反应后的红色固体中含氧化亚铜。已知:①Cu2O+H+=Cu2++Cu ②限选试剂:2mol/LH2SO4溶液、12mol/LH2SO4溶液、2mol/LHNO3溶液、10mol/LHNO3溶液

请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为______________________。
(2)反应过程中持续通入N2的作用有两点:一是使装置A中产生的氨气完全导出,二是____________。
(3)一段时间后,你认为装置F中可观察到什么现象?_______________________。
(4)用离子方程式解释装置G中溶液变成蓝色的原因:_______________________。
(5)反应完毕,装置C中的氧化铜完全反应,由黑色变为红色,称其质量为6.8g,且生成的气体可直接排放到大气中,则红色固体是_______,该反应中电子转移的物质的量为__________mol。
(6)请你设计一个实验方案,证明装置C中完全反应后的红色固体中含氧化亚铜。已知:①Cu2O+H+=Cu2++Cu ②限选试剂:2mol/LH2SO4溶液、12mol/LH2SO4溶液、2mol/LHNO3溶液、10mol/LHNO3溶液
| 实验步骤 | 预期现象和结论 |
| 步骤1:取装置C中反应后的少许固体于试管中 | |
| 步骤2:___________________________________ | ______________________________________ |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网