解答题-原理综合题 较难0.4 引用2 组卷454
1.钒的化合物常用于制作催化剂和新型电池。回答下列问题:
【小题1】金属钒可由铝热反应制得。已知25℃、101 kPa时,
4A1(s)+3O2(g)=2Al2O3(s) △H1=a kJ·mol-1
4V(s) +5O2(g)=2V2O5(s) △H2=b kJ·mol-1
则用铝热反应冶炼金属V(s)的热化学方程式为_____________________ 。
【小题2】V2O5为橙黄至砖红色固体,无味、有毒,微溶于水,是许多有机和无机反应的催化剂。下图表示的是25℃时,部分含钒微粒的存在形式、浓度和存在的pH范围(其余可溶性微粒均未标出),图中“[V]”表示含钒微粒的浓度,虚线表示[V]或pH的范围尚未准确确定。
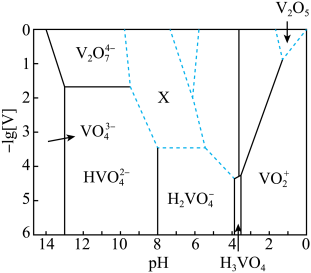
①V2O5溶于足量2mol • L-1NaOH溶液中,发生反应的离子方程式为_________________ ,向反应后的溶液中,滴加硫酸溶液至过量(pH<1)的过程中,开始溶液保持澄清,滴加一段时间后,观察到有橙黄色沉淀产生,继续滴加硫酸溶液,沉淀又消失。则沉淀消失过程中发生反应的化学方程式为_______________ 。
②上述滴加硫酸溶液的过程中,先后发生如下反应:
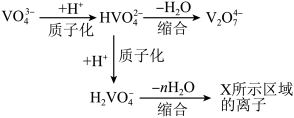
则“X所示区域溶液中的离子”不可能是___________ (填序号);
a.V3O b.V4O
b.V4O c. V4O
c. V4O
【小题3】V2O5是反应2SO2+O2 2SO3的催化剂。其他条件不变,加入V2O5后,该反应的速率加快的原因是
2SO3的催化剂。其他条件不变,加入V2O5后,该反应的速率加快的原因是_______________ ;恒温恒压下,加入V2O5,该反应的平衡常数________________ (填“增大”、 “减小”或“不变”);
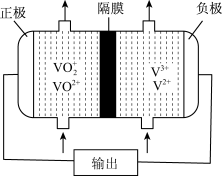
【小题4】下图所示为可充电的全钒液流电池构造示意图,该电池中的隔膜只允许H+通过。电池放电时,负极区溶液的pH将_____________ (填“增大”、“减小”或“不变”),电池充电时,阳极的电极反应式为_____________________ 。
【小题1】金属钒可由铝热反应制得。已知25℃、101 kPa时,
4A1(s)+3O2(g)=2Al2O3(s) △H1=a kJ·mol-1
4V(s) +5O2(g)=2V2O5(s) △H2=b kJ·mol-1
则用铝热反应冶炼金属V(s)的热化学方程式为
【小题2】V2O5为橙黄至砖红色固体,无味、有毒,微溶于水,是许多有机和无机反应的催化剂。下图表示的是25℃时,部分含钒微粒的存在形式、浓度和存在的pH范围(其余可溶性微粒均未标出),图中“[V]”表示含钒微粒的浓度,虚线表示[V]或pH的范围尚未准确确定。

①V2O5溶于足量2mol • L-1NaOH溶液中,发生反应的离子方程式为
②上述滴加硫酸溶液的过程中,先后发生如下反应:

则“X所示区域溶液中的离子”不可能是
a.V3O
【小题3】V2O5是反应2SO2+O2
【小题4】下图所示为可充电的全钒液流电池构造示意图,该电池中的隔膜只允许H+通过。电池放电时,负极区溶液的pH将

2017·山东济南·二模
类题推荐
钒是一种重要的合金元素,还用于催化剂和新型电池。从含钒固体废弃物(含有SiO2、Al2O3及其他残渣)中提取钒的一种新工艺主要流程如下:

部分含钒化合物在水中的溶解性如下表:
请回答下列问题:
(1)反应①所得溶液中除H+之外的阳离子有___________ 。
(2)反应②碱浸后滤出的固体主要成分是____________ (写化学式)。
(3)反应④的离子方程式为____________________ 。
(4)25℃、101 kPa时,4Al(s)+3O2(g)==2Al2O3(s) ΔH1=-a kJ/mol
4V(s)+5O2(g)==2V2O5(s) ΔH2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是_____________ 。
(5)钒液流电池(如右上图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过。电池放电时负极的电极反应式为__________ ,电池充电时阳极的电极反应式是_________ 。

(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2 +H2C2O4+2H+=2VO2++2CO2↑+2H2O。取25.00 mL0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为
+H2C2O4+2H+=2VO2++2CO2↑+2H2O。取25.00 mL0.1000 mol/LH2C2O4标准溶液于锥形瓶中,加入指示剂,将待测液盛放在滴定管中,滴定到终点时消耗待测液24.0 mL,由此可知,该(VO2)2SO4溶液中钒的含量为______ g/L。

部分含钒化合物在水中的溶解性如下表:
| 物质 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
| 溶解性 | 难溶 | 难溶 | 可溶 | 易溶 |
(1)反应①所得溶液中除H+之外的阳离子有
(2)反应②碱浸后滤出的固体主要成分是
(3)反应④的离子方程式为
(4)25℃、101 kPa时,4Al(s)+3O2(g)==2Al2O3(s) ΔH1=-a kJ/mol
4V(s)+5O2(g)==2V2O5(s) ΔH2=-b kJ/mol
用V2O5发生铝热反应冶炼金属钒的热化学方程式是
(5)钒液流电池(如右上图所示)具有广阔的应用领域和市场前景,该电池中隔膜只允许H+通过。电池放电时负极的电极反应式为

(6)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应①后溶液中的含钒量,反应的离子方程式为:2
磷酸是重要的化学试剂和工业原料。请回答下列问题:
(1)已知:25°C时,磷酸和碳酸的电离常数如下表所示。
向Na2CO3溶液中滴加少量H3PO4溶液,反应的离子方程式为__ 。
(2)已知:
I.CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ∆H= -271kJ·mol-1
II.5CaO(s)+3H3PO4(l)+HF(g)=Ca3(PO4)3F(s)+5H2O(l) ∆H=-937 kJ·mol-1
回答下列问题:
①工业上用Ca3(PO4)3F和硫酸反应制备磷酸的热化学方程式为__ 。
②一定条件下,在密闭容器中只发生反应II,达到平衡后缩小容器容积,HF的平衡转化率__ (填“增大”“减小”或“不变”,下同);HF的平衡浓度__ 。
(3)工业上用磷尾矿制备Ca3(PO4)3F时生成的副产物CO可用于制备H2,原理为CO(g)+H2O(g)=CO2(g)+H2(g) ∆H。
①一定温度下,向10L密闭容器中充入0.5molCO和lmolH2O(g),2min达到平衡时,测得0~2min内用CO2表示的反应速率v(CO2)=0.02mol·L-1·min-1。则CO的平衡转化率a=__ ,该反应的平衡常数K=__ 。
②在压强不变的密闭容器中发生上述反应,设起始的 =y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的∆H
=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的∆H__ 0(填“>”“<”或“=”,下同)。a_ 1,理由为__ 。

(1)已知:25°C时,磷酸和碳酸的电离常数如下表所示。
物质 | H3PO4 | H2CO3 |
电离常数 | Ka1=7.1×10-3 Ka2= 6.3×10-8 Ka3= 4.2×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
(2)已知:
I.CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ∆H= -271kJ·mol-1
II.5CaO(s)+3H3PO4(l)+HF(g)=Ca3(PO4)3F(s)+5H2O(l) ∆H=-937 kJ·mol-1
回答下列问题:
①工业上用Ca3(PO4)3F和硫酸反应制备磷酸的热化学方程式为
②一定条件下,在密闭容器中只发生反应II,达到平衡后缩小容器容积,HF的平衡转化率
(3)工业上用磷尾矿制备Ca3(PO4)3F时生成的副产物CO可用于制备H2,原理为CO(g)+H2O(g)=CO2(g)+H2(g) ∆H。
①一定温度下,向10L密闭容器中充入0.5molCO和lmolH2O(g),2min达到平衡时,测得0~2min内用CO2表示的反应速率v(CO2)=0.02mol·L-1·min-1。则CO的平衡转化率a=
②在压强不变的密闭容器中发生上述反应,设起始的

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网





