解答题-原理综合题 适中0.65 引用1 组卷541
FeCl3的用途广泛。
(1)实验室利用FeCl3制备Fe(OH)3胶体:
①Fe(OH)3胶体制备反应的化学方程式为___________________________________________ 。
②利用所制得的Fe(OH)3胶体进行实验:将其装入U形管内,用石墨作电极,通电一段时间后发现
___________ 极区附近的红褐色逐渐变深,这表明_________________________________
③向Fe(OH)3胶体中加H2SO4溶液,产生的现象是_______________________________ 。
(2)FeCl3溶液常用于腐蚀铜印刷电路板,该反应的离子方程式为_________________________ 。
(3)FeCl3常用于净水,用离子方程式表示其原理____________________________________ 。
(4)FeCl3溶液中若混有FeCl2,检验FeCl2的试剂为________________________ 。
(5)将FeCl3溶液蒸干并灼烧得到的固体成分为__________________ 。
(6)已知Fe(OH)3的Ksp=8×10-38,某溶液中c(FeCl3)=0.05mol/L,如果要使Fe(OH)3沉淀完全,pH至少为______________________ 。
(溶液中离子浓度小于10-5mol/L认为沉淀已完全,已知lg2=0.3 lg5=0.7)
(1)实验室利用FeCl3制备Fe(OH)3胶体:
①Fe(OH)3胶体制备反应的化学方程式为
②利用所制得的Fe(OH)3胶体进行实验:将其装入U形管内,用石墨作电极,通电一段时间后发现
③向Fe(OH)3胶体中加H2SO4溶液,产生的现象是
(2)FeCl3溶液常用于腐蚀铜印刷电路板,该反应的离子方程式为
(3)FeCl3常用于净水,用离子方程式表示其原理
(4)FeCl3溶液中若混有FeCl2,检验FeCl2的试剂为
(5)将FeCl3溶液蒸干并灼烧得到的固体成分为
(6)已知Fe(OH)3的Ksp=8×10-38,某溶液中c(FeCl3)=0.05mol/L,如果要使Fe(OH)3沉淀完全,pH至少为
(溶液中离子浓度小于10-5mol/L认为沉淀已完全,已知lg2=0.3 lg5=0.7)
16-17高二下·黑龙江哈尔滨·期中
类题推荐
从某废液(含有Fe3+、Fe2+、Cu2+、Cl-)中回收铜并制得纯净的FeCl3溶液。现以制得的纯净的FeCl3溶液为原料制取优良的水处理剂高铁酸钾(K2FeO4),其流程如图:
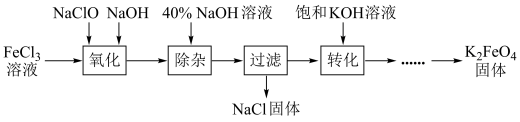
已知:高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定;具有强氧化性;与水作用产生Fe(OH)3。
(1)高铁酸钾(K2FeO4)在处理水过程中的作用是_________ 和_________ 。
(2)检验废液中含有Fe2+选用的试剂是__________ (填化学式)。
(3)“氧化”过程反应的离子方程式为__________ 。
(4)上述工艺得到的高铁酸钾常含有杂质,可用重结晶法提纯,操作是将粗产品用______ 溶解,然后______ ,过滤。
(5)用回收的铜为原料可制得粗CuSO4·5H2O晶体(含有少量的FeSO4·7H2O),除去CuSO4·5H2O晶体中杂质的方法是将该晶体溶于水,向溶液中加入H2O2,再调节溶液pH。过滤即可制得纯净的CuSO4溶液,进而可制得纯净的CuSO4·5H2O晶体。
已知:室温时一些物质的Ksp如表所示:
已知溶液中的某离子浓度小于1×10-5 mol/L时就认为该离子沉淀完全。加双氧水的目的是_________ ;若溶液中CuSO4的浓度为3.0mol/L,通过计算说明此方法可除去粗CuSO4·5H2O晶体中FeSO4·7H2O的理由:___________ 。

已知:高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,在中性或酸性溶液中逐渐分解,在碱性溶液中稳定;具有强氧化性;与水作用产生Fe(OH)3。
(1)高铁酸钾(K2FeO4)在处理水过程中的作用是
(2)检验废液中含有Fe2+选用的试剂是
(3)“氧化”过程反应的离子方程式为
(4)上述工艺得到的高铁酸钾常含有杂质,可用重结晶法提纯,操作是将粗产品用
(5)用回收的铜为原料可制得粗CuSO4·5H2O晶体(含有少量的FeSO4·7H2O),除去CuSO4·5H2O晶体中杂质的方法是将该晶体溶于水,向溶液中加入H2O2,再调节溶液pH。过滤即可制得纯净的CuSO4溶液,进而可制得纯净的CuSO4·5H2O晶体。
已知:室温时一些物质的Ksp如表所示:
| 化学式 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
| Ksp | 8.0×10-16 | 8.0×10-38 | 3×10-20 |
铁、铜及其化合物在日常生活及工业生产中用途非常广泛。
I.FeCl3是常用的金属蚀刻剂和净水剂。
(1)FeCl3净水的原理是___ (用离子方程式及语言表示)。
(2)FeCl3在溶液中分三步水解:Fe3++H2O Fe(OH)2++H+ K1;Fe(OH)2++H2O
Fe(OH)2++H+ K1;Fe(OH)2++H2O Fe(OH)
Fe(OH) +H+ K2;Fe(OH)
+H+ K2;Fe(OH) +H2O
+H2O Fe(OH)3+H+ K3。以上水解反应的平衡常数K1、K2、K3由大到小的顺序是
Fe(OH)3+H+ K3。以上水解反应的平衡常数K1、K2、K3由大到小的顺序是___ 。
(3)配制FeCl3溶液时,常将FeCl3晶体溶于浓盐酸中,使用时加蒸馏水稀释至指定浓度。某同学误将FeCl3直接放入自来水中(含有Mg2+、Ca2+、HCO 、Cl-等杂质离子),看到红褐色沉淀和大量气泡,试解释出现该现象的原因
、Cl-等杂质离子),看到红褐色沉淀和大量气泡,试解释出现该现象的原因___ (用离子方程式表示)。
II.CuCl2常用作电镀添加剂、催化剂及饲料添加剂。
(4)①25℃时Fe(OH)2、Fe(OH)3、Cu(OH)2的Ksp如表所示,计算当溶液中Fe2+、Cu2+浓度均为0.1mol/L时,Fe(OH)2沉淀完全及Cu(OH)2开始沉淀时的pH值(已知lg2=0.3,离子浓度小于1.0×10-5mol/L视为沉淀完全)。
②为了除去CuCl2溶液中含有的少量FeCl2,可以用氧化剂将FeCl2氧化为FeCl3,调控溶液pH___ (填范围),将FeCl3转化为Fe(OH)3除去。
I.FeCl3是常用的金属蚀刻剂和净水剂。
(1)FeCl3净水的原理是
(2)FeCl3在溶液中分三步水解:Fe3++H2O
(3)配制FeCl3溶液时,常将FeCl3晶体溶于浓盐酸中,使用时加蒸馏水稀释至指定浓度。某同学误将FeCl3直接放入自来水中(含有Mg2+、Ca2+、HCO
II.CuCl2常用作电镀添加剂、催化剂及饲料添加剂。
(4)①25℃时Fe(OH)2、Fe(OH)3、Cu(OH)2的Ksp如表所示,计算当溶液中Fe2+、Cu2+浓度均为0.1mol/L时,Fe(OH)2沉淀完全及Cu(OH)2开始沉淀时的pH值(已知lg2=0.3,离子浓度小于1.0×10-5mol/L视为沉淀完全)。
| 分子式 | Ksp | 开始沉淀时的pH | 沉淀完全时的pH |
| Fe(OH)2 | 4.0×10-17 | 6.3 | a= |
| Fe(OH)3 | 2.79×10-39 | 1.5 | 2.8 |
| Cu(OH)2 | 1.6×10-20 | b= | 6.6 |
②为了除去CuCl2溶液中含有的少量FeCl2,可以用氧化剂将FeCl2氧化为FeCl3,调控溶液pH
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



