填空题 适中0.65 引用2 组卷238
(1)CH3COOH是最常见的有机弱酸。
①CH3COOH的电离方程式为_____________ 。
②CH3COONa溶液呈碱性,原因是__________ (填“CH3COO-”或“Na+”)水解引起的。
③在CH3COONa溶液中,c(Na+)_______ c(CH3COO-)(填“>”“=”或“<”)。
(2)已知:反应C(s)+H2O(g) CO(g)+H2(g)的△H=131.3kJ/mol。
CO(g)+H2(g)的△H=131.3kJ/mol。
①该反应是反应__________ (填“吸热”或“放热”)。
②若反应消耗24g C(s),则反应的热效应为__________ 。
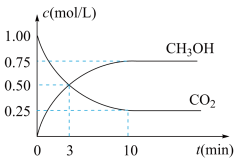
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol通入容积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
① 2min内,v(CO)=__________ 。
②该温度下,此反应的平衡常数表达式K=_________ 。
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数_____ (填“增大”、“减小”或“不变”)。
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极,请回答下列问题:
① C1作_________ (填“阳极”或”阴极”)。
② C2极电极反应式为____________ 。
①CH3COOH的电离方程式为
②CH3COONa溶液呈碱性,原因是
③在CH3COONa溶液中,c(Na+)
(2)已知:反应C(s)+H2O(g)
 CO(g)+H2(g)的△H=131.3kJ/mol。
CO(g)+H2(g)的△H=131.3kJ/mol。①该反应是反应
②若反应消耗24g C(s),则反应的热效应为
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol通入容积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:t/min | 2 | 4 | 7 | 9 |
n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
① 2min内,v(CO)=
②该温度下,此反应的平衡常数表达式K=
③其他条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数
(4)下图为直流电源电解CuSO4溶液的装置,C1和C2都为石墨电极,请回答下列问题:
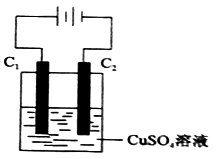
① C1作
② C2极电极反应式为
2017高二·湖南·学业考试
类题推荐
碳及其化合物有广泛的用途。
(1)反应C(s)+H2O(g) CO(g)+H2(g)ΔH=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g)+H2(g)ΔH=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
(2)已知,C(s)+CO2(g) 2CO(g)△H=+172.5kJ•mol-1
2CO(g)△H=+172.5kJ•mol-1
则反应CO(g)+H2O(g) CO2(g)+H2(g)的△H= kJ•mol-1。
CO2(g)+H2(g)的△H= kJ•mol-1。
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
①其它条件不变,降低温度,达到新平衡前v(逆)__________v(正)(填“>”、“<”或“="”)" 。
②该温度下,此反应的平衡常数K= ;
③其它条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数______(填“增大”、 “减小”或“不变”)。
(1)反应C(s)+H2O(g)
 CO(g)+H2(g)ΔH=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g)+H2(g)ΔH=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。| A.增加碳的用量 | B.升高温度 | C.用CO吸收剂除去CO | D.加入催化剂 |
(2)已知,C(s)+CO2(g)
 2CO(g)△H=+172.5kJ•mol-1
2CO(g)△H=+172.5kJ•mol-1则反应CO(g)+H2O(g)
 CO2(g)+H2(g)的△H= kJ•mol-1。
CO2(g)+H2(g)的△H= kJ•mol-1。(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:| t / min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
①其它条件不变,降低温度,达到新平衡前v(逆)__________v(正)(填“>”、“<”或“="”)" 。
②该温度下,此反应的平衡常数K= ;
③其它条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数______(填“增大”、 “减小”或“不变”)。
碳及其化合物有广泛的用途。
(1)反应C(s)+ H2O(g) CO(g)+H2(g) ΔH=" +131.3" kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g)+H2(g) ΔH=" +131.3" kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
(2)已知,C(s)+ CO2(g) 2CO(g) △H=+172.5kJ•mol-1
2CO(g) △H=+172.5kJ•mol-1
则反应 CO(g)+H2O(g) CO2(g)+H2(g) 的△H= kJ•mol-1。
CO2(g)+H2(g) 的△H= kJ•mol-1。
(3)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
① 其它条件不变,降低温度,达到新平衡前v(逆)_________v(正)(填“>”、“<”或“="”)" 。
② 该温度下,此反应的平衡常数K=___________;
③ 其它条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数______(填“增大”、“减小”或“不变”)。
(1)反应C(s)+ H2O(g)
 CO(g)+H2(g) ΔH=" +131.3" kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g)+H2(g) ΔH=" +131.3" kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。| A.增加碳的用量 | B.升高温度 |
| C.用CO吸收剂除去CO | D.加入催化剂 |
(2)已知,C(s)+ CO2(g)
 2CO(g) △H=+172.5kJ•mol-1
2CO(g) △H=+172.5kJ•mol-1则反应 CO(g)+H2O(g)
 CO2(g)+H2(g) 的△H= kJ•mol-1。
CO2(g)+H2(g) 的△H= kJ•mol-1。(3)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:| t / min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
① 其它条件不变,降低温度,达到新平衡前v(逆)_________v(正)(填“>”、“<”或“="”)" 。
② 该温度下,此反应的平衡常数K=___________;
③ 其它条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数______(填“增大”、“减小”或“不变”)。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网