解答题-原理综合题 较难0.4 引用1 组卷189
铜及其化合物具有广泛的应用。回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子的基态核外电子排布式为__________ ,S、O、N三种元素的第一电离能由大到小的顺序为___________________ 。
(2)Cu(NO3)2溶液中通入足量NH3能生成配合物[Cu(NH3)4](NO3)2。其中NH3中心原子的杂化轨道类型为________ ,[Cu(NH3)4](NO3)2中存在的化学键除了极性共价键外,还有___________ 。
(3)CuSO4溶液中加入过量KCN能生成配离子[Cu(CN)4]2-,1mol CN‑中含有的π键数目为_____________ 。与CN-互为等电子体的离子有_________ (写出一种即可)。
(4)CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因可能是_______________________________ 。
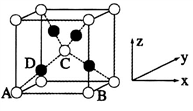
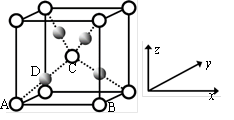
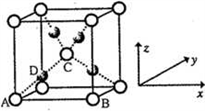
(5)已知Cu2O晶胞结构如图所示:该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);c为 。则D原子的坐标参数为
。则D原子的坐标参数为__________ ,它代表_________ 原子(填元素符号)。
(6)金属铜是面心立方最密堆积方式,则晶体中铜原子的配位数是_______ ,该晶胞中Cu原子的空间利用率是__________ 。
(1)CuSO4和Cu(NO3)2中阳离子的基态核外电子排布式为
(2)Cu(NO3)2溶液中通入足量NH3能生成配合物[Cu(NH3)4](NO3)2。其中NH3中心原子的杂化轨道类型为
(3)CuSO4溶液中加入过量KCN能生成配离子[Cu(CN)4]2-,1mol CN‑中含有的π键数目为
(4)CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因可能是

(5)已知Cu2O晶胞结构如图所示:该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);c为
(6)金属铜是面心立方最密堆积方式,则晶体中铜原子的配位数是
2017·山东泰安·二模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网