填空题 适中0.65 引用2 组卷585
共价键都有键能之说,键能是指拆开1 mol共价键所需要吸收的能量或形成1mol共价键所放出的能量。
(1)已知H—Cl键的键能为431.4 kJ/mol,下列关于键能的叙述正确的是______________。
(2)参考下表中的数据,判断下列分子受热时最稳定的是___________。
(3)能用键能大小解释的是____________。
(4)已知:4HCl+O2=2Cl2+2H2O,常温下,4mol HCl被氧化,放出115.6kJ的热量.写出该反应的热化学方程式_____________________ .
(5)在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的ΔH表示生成1mol产物的数据)
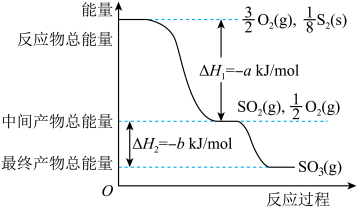
①写出表示S8燃烧热的热化学方程式:______________ .
②写出SO3分解生成SO2和O2的热化学方程式:______________ .
(1)已知H—Cl键的键能为431.4 kJ/mol,下列关于键能的叙述正确的是______________。
| A.每生成1 mol H—Cl键吸收431.4 kJ能量 |
| B.每生成1 mol H—Cl键放出431.4 kJ能量 |
| C.每拆开1 mol H—Cl键放出431.4 kJ能量 |
| D.每拆开1 mol H—Cl键吸收431.4 kJ能量 |
化学键 | H—H | H—F | H—Cl | H—Br |
键能/kJ/mol | 436 | 565 | 431 | 368 |
| A.H2 | B.HF | C.HCl | D.HBr |
| A.常温常压下,溴呈液态,碘呈固态 | B.氮气的化学性质比氧气稳定 |
| C.稀有气体一般很难发生化学反应 | D.硝酸易挥发而硫酸难挥发 |
(5)在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的ΔH表示生成1mol产物的数据)

①写出表示S8燃烧热的热化学方程式:
②写出SO3分解生成SO2和O2的热化学方程式:
16-17高一下·辽宁沈阳·阶段练习
类题推荐
共价键都有键能之说,键能是指拆开1 mol共价键所需要吸收的能量或形成1 mol共价键所放出的能量。
(1)参考下表中的数据,判断下列分子受热时最稳定的是_______。
(2)能用键能大小解释的是_______。
(3)在一定条件下, 和
和 发生反应依次转化为
发生反应依次转化为 和
和 。反应过程和能量关系可用如图简单表示(图中的
。反应过程和能量关系可用如图简单表示(图中的 表示生成1 mol产物的数据)
表示生成1 mol产物的数据)
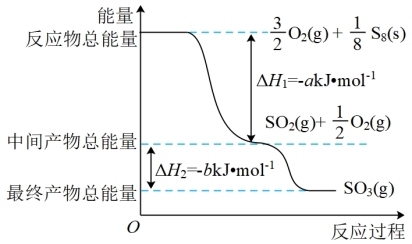
写出表示S燃烧热的热化学方程式:_______ 。
(4)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量,请回答下列问题:
①该反应的热化学方程式为_______ 。
②若1 mol氢气完全燃烧生成1 mol气态水放出241 kJ的热量,已知 键键能为
键键能为 ,
, 键键能为
键键能为 ,计算
,计算 键键能为
键键能为_______  。
。
(5)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金 ,已知:
,已知:

 ;
;

 ;
;

 。
。
则
_______  。
。
(6)300℃时, 的正反应速率表达式为
的正反应速率表达式为 ,测得速率和浓度的关系如下表:
,测得速率和浓度的关系如下表:
由表中数据可知,
_______ ;
_______ 。
(1)参考下表中的数据,判断下列分子受热时最稳定的是_______。
| 化学键 | ||||
| 键能/ | 436 | 565 | 431 | 368 |
| A. | B.HF | C.HCl | D.HBr |
| A.常温常压下,溴呈液态,碘呈固态 | B.氮气的化学性质比氧气稳定 |
| C.稀有气体一般很难发生化学反应 | D.硝酸易挥发而硫酸难挥发 |

写出表示S燃烧热的热化学方程式:
(4)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量,请回答下列问题:
①该反应的热化学方程式为
②若1 mol氢气完全燃烧生成1 mol气态水放出241 kJ的热量,已知
(5)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金
则
(6)300℃时,
| 序号 | ||
| ① | 0.30 | |
| ② | 0.60 | |
| ③ | 0.90 |
下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJ·mol−1)。回答问题
(1)下列关于键能的叙述正确的是___________(填字母,下同)。
(2)已知热化学方程式:H2(g)+Cl2(g)=2HCl(g) ΔH=-183kJ·mol−1,则Cl2的键能为___________ kJ·mol−1。
(3)参考下表中的数据,判断下列分子受热时最稳定的是___________。
(4)能用键能大小解释的是___________。
| 化学键 | H-H | H-Cl |
| 键能 | 436 | 431 |
| A.每生成1molH-Cl吸收431.4kJ能量 |
| B.每生成1molH-Cl放出431.4kJ能量 |
| C.每拆开1molH-Cl放出431.4kJ能量 |
| D.每拆开1molH-Cl吸收431.4kJ能量 |
(3)参考下表中的数据,判断下列分子受热时最稳定的是___________。
| 化学键 | H-H | H-F | H-Cl | H-Br |
| 键能/(kJ·mol-1) | 436 | 565 | 431 | 368 |
| A.H2 | B.HF | C.HCl | D.HBr |
| A.常温常压下,溴呈液态,碘呈固态 | B.氮气的化学性质比氧气稳定 |
| C.稀有气体一般很难发生化学反应 | D.硝酸易挥发而硫酸难挥发 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



