解答题-实验探究题 适中0.65 引用1 组卷128
碱式碳酸镁可用于牙膏、医药化妆品等工业,化学式为4MgCO3·Mg(OH)2·5H2O,某碱式碳酸镁中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下几个方案:
方案1
取一定质量的样品,与硫酸充分反应,通过测定CO2的质量计算纯度
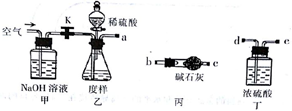
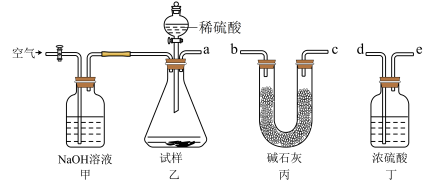
(1)乙中发生反应的方程式为______________________________ 。
(2)仪器接口的连接顺序为(装置可以重复使用) a___________ ,丁的作用是__________________ 。
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是______________________________ 。
方案Ⅱ
①称取碱式碳酸镁样品mg;②将样品充分高温燃烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用托盘天平称量)。
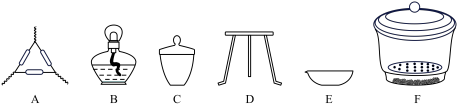
(4)下列仪器中,该方案不会用到的是____________ 。
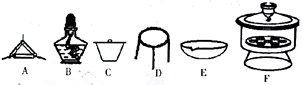
(5)判断样品完全分解的方法是_________________________ 。
(6)有同学认为方案Ⅱ高温燃烧的过程中会发生
会导致测定结果有误,你任为这位同学的观点正确吗?_________ ,(填“正确”或“错误”)
请说明自己的理由:______________________ 。
方案1
取一定质量的样品,与硫酸充分反应,通过测定CO2的质量计算纯度

(1)乙中发生反应的方程式为
(2)仪器接口的连接顺序为(装置可以重复使用) a
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是
方案Ⅱ
①称取碱式碳酸镁样品mg;②将样品充分高温燃烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用托盘天平称量)。
(4)下列仪器中,该方案不会用到的是

(5)判断样品完全分解的方法是
(6)有同学认为方案Ⅱ高温燃烧的过程中会发生

会导致测定结果有误,你任为这位同学的观点正确吗?
请说明自己的理由:
2017·湖南郴州·三模
类题推荐
某碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下方案:①称取碱式碳酸镁样品mg;②将样品充分高温煅烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用电子天平称量)。
(1)下列仪器中,该方案不会用到的是________ 。___________ ;本实验至少需要称量___________ 次。
(3)某研究小组进行三次实验,数据记录如下:
通过计算,该样品中碱式碳酸镁的纯度为___________ 。(4MgCO3·Mg(OH)2·4H2O式量466;写出简要的步骤)
(4)有同学认为高温煅烧过程中会发生MgCO3+SiO2 MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?
MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?___________ (填“正确”或“错误”),请说明自己的理由:___________ 。
(1)下列仪器中,该方案不会用到的是
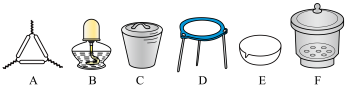
(3)某研究小组进行三次实验,数据记录如下:
| 样品质量/g | 剩余固体质量/g | |
| 实验1 | 18.000 | 8.000 |
| 实验2 | 18.000 | 8.020 |
| 实验3 | 18.000 | 7.980 |
(4)有同学认为高温煅烧过程中会发生MgCO3+SiO2
某兴趣小组为测定某工业纯碱(假设仅含碳酸氢钠杂质)中碳酸钠的质量分数,设计了下列三种实验方案进行探究。请填空:
方案一:纯碱样品经加热后测定剩余固体质量,并计算碳酸钠的质量分数。
(1)加热样品所选用的仪器是____ (填标号)。
(2)加热时发生反应的化学方程式是______ 。
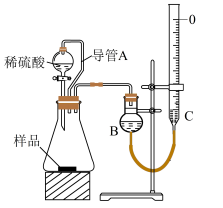
方案二:将一定质量的样品与足量稀硫酸反应,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差计算碳酸钠的质量分数。实验装置如图:
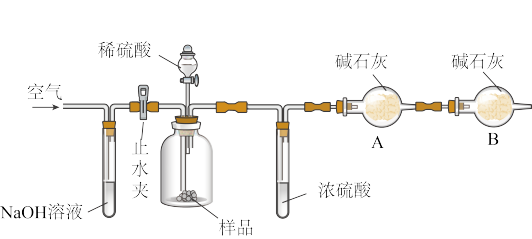
该实验的操作步骤:
①关闭止水夹,在干燥管内填满碱石灰,称量干燥管A质量
②取一定量样品装入广口瓶中
③检查装置的气密性
④打开止水夹,缓慢鼓入空气数分钟,再称量干燥管A质量
⑤缓慢加入稀硫酸至不再产生气体为止
⑥打开止水夹,缓慢鼓入空气数分钟
(3)正确的操作顺序是____ (填序号)
(4)在操作④中,要缓慢鼓入空气数分钟,鼓入空气的作用是____ 。
方案三:利用化学反应把HCO 、CO
、CO 完全转化为沉淀,称量沉淀的质量,计算碳酸钠的质量分数。
完全转化为沉淀,称量沉淀的质量,计算碳酸钠的质量分数。
(5)称取mg样品,置于小烧杯中,加水溶解,滴加足量沉淀剂,把溶液中HCO 、CO
、CO 完全转化为沉淀,应选用的沉淀剂是
完全转化为沉淀,应选用的沉淀剂是____ (填标号)。
(6)将沉淀洗涤,并充分干燥,称量沉淀的质量为m2g,由此可以计算碳酸钠的质量分数。如果此步骤中,沉淀未干燥充分就称量,则所测碳酸钠的质量分数____ (填“偏大”“偏小”或“无影响”)。
方案一:纯碱样品经加热后测定剩余固体质量,并计算碳酸钠的质量分数。
(1)加热样品所选用的仪器是
A.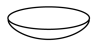 | B.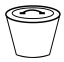 | C.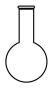 | D.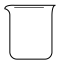 |
方案二:将一定质量的样品与足量稀硫酸反应,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差计算碳酸钠的质量分数。实验装置如图:

该实验的操作步骤:
①关闭止水夹,在干燥管内填满碱石灰,称量干燥管A质量
②取一定量样品装入广口瓶中
③检查装置的气密性
④打开止水夹,缓慢鼓入空气数分钟,再称量干燥管A质量
⑤缓慢加入稀硫酸至不再产生气体为止
⑥打开止水夹,缓慢鼓入空气数分钟
(3)正确的操作顺序是
(4)在操作④中,要缓慢鼓入空气数分钟,鼓入空气的作用是
方案三:利用化学反应把HCO
(5)称取mg样品,置于小烧杯中,加水溶解,滴加足量沉淀剂,把溶液中HCO
| A.CaCl2溶液 | B.MgSO4溶液 | C.NaCl溶液 | D.Ba(OH)2溶液 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网