解答题-结构与性质 适中0.65 引用1 组卷131
X、Y、Z、W、M、N是元素周期表中前四周期原子序数依次增大的六种元素,其相关信息如下表:
(1)红色金属N位于元素周期表中的位置为______________ ,其基态原子的电子排布式为_______________
(2)H2Y分子的立体构型为_____ 形,XY2分子中X原子的杂化轨道的类型是______ ,与XY分子互为等电子体的微粒有__________________ (写一种即可,填化学式)
(3)Y单质和Z单质点燃条件下得到的固体产物为________ (填化学式),其晶体类型为___________ 晶体
(4)与Z同周期且相邻的两种元素的原子与Z比较,三者第一电离能最大的为______ ,X、Y两种元素电负性的大小关系为_____ >_____ (均用元素符号表示)。
(5)写出N的单质在潮湿的空气中生成绿色锈斑的化学方程式__________
(6)W与Y元素同主族且相邻,W的单质在空气中燃烧生成一种无色有刺激性气味的气体。该气体与含1.5 mol M的一种含氧酸(该酸的钾盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式是:______________________ 。
元素 | 相关信息 |
X | X的基态原子核外只有三个能级,且各能级电子数相等 |
Y | Ne与Y2-的核外电子数相同 |
Z | Z的基态原子价电子排布为nsn-1 |
N | N的单质是一种常见的红色金属,在潮湿的空气中易生成绿色的锈斑 |
(1)红色金属N位于元素周期表中的位置为
(2)H2Y分子的立体构型为
(3)Y单质和Z单质点燃条件下得到的固体产物为
(4)与Z同周期且相邻的两种元素的原子与Z比较,三者第一电离能最大的为
(5)写出N的单质在潮湿的空气中生成绿色锈斑的化学方程式
(6)W与Y元素同主族且相邻,W的单质在空气中燃烧生成一种无色有刺激性气味的气体。该气体与含1.5 mol M的一种含氧酸(该酸的钾盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式是:
16-17高二上·重庆·期末
类题推荐
X、Y、Z、W是元素周期表中前四周期原子序数依次增大的四种元素:
(1)W位于元素周期表第________ 周期第__________ 族,其基态原子价电子排布式为__________
(2)与Z同周期且依次相邻的两种元素的原子与Z比较,三者第一电离能的大小顺序为________ (用元素符号表示);Y的氢化物在同族的氢化物中沸点反常,其原因是_________________ 。
(3)XY2的电子式为______ ,该分子的形状为_________ ,含有_____ 个σ键和_________ 个π键。
(4)写出W的单质在潮湿的空气中生成绿色锈斑的化学方程式,并标出电子转移的方向和数目________ 。
| 元素 | 相关信息 |
| X | X的基态原子核外只有三个能级,且各能级电子数相等 |
| Y | Y的基态原子最外层电子数是其内层电总子数的3倍 |
| Z | Z的基态原子价电子排布为nsn-1 |
| W | W的单质是一种常见的红色金属,在潮湿的空气中易生成绿色的锈斑 |
(2)与Z同周期且依次相邻的两种元素的原子与Z比较,三者第一电离能的大小顺序为
(3)XY2的电子式为
(4)写出W的单质在潮湿的空气中生成绿色锈斑的化学方程式,并标出电子转移的方向和数目
X、Y、Z、W、E、M是元素周期表前四周期中的常见元素,且原子序数依次增大,相关信息如下,请回答下列问题:
(1)Y元素基态原子中能量最高的电子其原子轨道呈___________ 形。Z元素的气态氢化物在同族元素的气态氢化物中沸点最高,原因是___________ 。
(2)X、Y、Z三种元素基态原子的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)Y、Z、W简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(4) 分子的空间结构为
分子的空间结构为___________ ,其中Y原子采取___________ 杂化。 易溶于水的原因有
易溶于水的原因有___________ (答出2点)。
(5)E在元素周期表中的位置为第___________ 周期第___________ 族,基态 价层电子的轨道表示式为
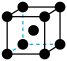
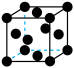
价层电子的轨道表示式为___________ 。X射线衍射实验测定,常见的E单质有两种晶胞,其结构如图所示。晶胞A中每个E原子紧邻的原子数为___________ ,每个晶胞B中含有的E原子数为___________ 。
(6)M属于___________ 区元素,其基态原子的价层电子排布式为___________ 。
| 元素 | 相关信息 |
| X | 基态原子的价电子排布式为 |
| Y | 元素原子的核外p电子数比s电子数少1个 |
| Z | 原子核外s能级电子总数与p能级电子总数相等,但第一电离能低于同周期相邻两元素 |
| W | 原子核外s能级电子总数与p能级电子总数相等,但第一电离能高于同周期相邻两元素 |
| E | 基态原子价电子层中的未成对电子数为4 |
| M | 基态原子核外最外层只有一个电子,其次外层内所有轨道的电子均成对 |
(1)Y元素基态原子中能量最高的电子其原子轨道呈
(2)X、Y、Z三种元素基态原子的第一电离能由大到小的顺序为
(3)Y、Z、W简单离子的半径由大到小的顺序为
(4)
(5)E在元素周期表中的位置为第
|
|
| 晶胞A | 晶胞B |
(6)M属于
X、Y、Z、W、J是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是 .
(2)元素Y位于元素周期表第 周期第 族.
(3)元素Z的原子最外层共有 种不同运动状态的电子.
(4)W的基态原子核外电子排布式是 .W的基态原子核外价电子排布图是 .
(5)元素Y与元素Z相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 .
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
(6)Y、Z两元素的最高价氧化物对应的水化物的酸性强弱为 (用化学式表示).比较下列物质的酸性强弱:HZO HZO3 HZO4.
(7)J的气态氢化物中心原子的杂化方式是 ,与该原子形成的单质分子互为等电子体的常见分子的分子式为 .
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
| J | J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐 |
(2)元素Y位于元素周期表第 周期第 族.
(3)元素Z的原子最外层共有 种不同运动状态的电子.
(4)W的基态原子核外电子排布式是 .W的基态原子核外价电子排布图是 .
(5)元素Y与元素Z相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 .
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
(6)Y、Z两元素的最高价氧化物对应的水化物的酸性强弱为 (用化学式表示).比较下列物质的酸性强弱:HZO HZO3 HZO4.
(7)J的气态氢化物中心原子的杂化方式是 ,与该原子形成的单质分子互为等电子体的常见分子的分子式为 .
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网