解答题-结构与性质 较难0.4 引用2 组卷476
人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、二氧化碳、青霉素、硝酸钾、乙醇、氨等“分子”改变过人类的世界。
(1)铁原子在基态时,外围电子排布式为____________ 。
(2)CO2的电子式为____________ ,1 mol CO2分子中含有σ键的物质的量为____________ 。
(3)6-氨基青霉烷酸的结构如图所示:
①其中C、N、O原子半径的大小关系为____________ ,电负性的大小关系为____________ ;
②其中采用sp3杂化的原子有C、____________ 。
(4)硝酸钾中NO3-的空间构型为____________ ,写出与NO3-互为等电子体的一种由前二周期元素原子构成的非极性分子化学式____________ 。
(5)乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是____________ 。
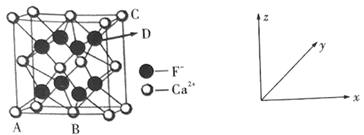
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若两个最近的Fe原子间的距离为a cm,则该晶体的密度计算式为____________ g/cm3(用NA表示阿伏伽德罗常数)。
(1)铁原子在基态时,外围电子排布式为
(2)CO2的电子式为
(3)6-氨基青霉烷酸的结构如图所示:
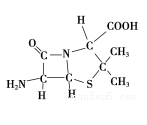
①其中C、N、O原子半径的大小关系为
②其中采用sp3杂化的原子有C、
(4)硝酸钾中NO3-的空间构型为
(5)乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若两个最近的Fe原子间的距离为a cm,则该晶体的密度计算式为

2017·吉林长春·二模
类题推荐
【化学——选修3:物质结构与性质】 人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化碳、聚乙烯、二氧化硅等17种“分子”改变过人类的世界。
(1)铁原子在基态时,价电子(外围电子)排布式为_______________________ 。
(2)硝酸钾中NO3-的空间构型为____________________ ,写出与NO3-互为等电子体的一种非极性分子化学式_______________ 。
(3)6氨基青霉烷酸的结构如图所示,其中采用sp3杂化的原子有____________ 。
(4)下列说法正确的有______________ (填字母序号)。
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(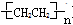 )分子中有5n个σ键
)分子中有5n个σ键
d.由下表中数据可确定在反应Si(s)+O2(g)===SiO2(s)中,每生成60 g SiO2放出的能量为(2c-a-b) kJ
(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式________________ 。若两个最近的Fe原子间的距离为s cm,则该晶体的密度是____________ g·mol-1。


(1)铁原子在基态时,价电子(外围电子)排布式为
(2)硝酸钾中NO3-的空间构型为
(3)6氨基青霉烷酸的结构如图所示,其中采用sp3杂化的原子有
(4)下列说法正确的有
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(
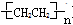 )分子中有5n个σ键
)分子中有5n个σ键d.由下表中数据可确定在反应Si(s)+O2(g)===SiO2(s)中,每生成60 g SiO2放出的能量为(2c-a-b) kJ
| 化学键 | Si—Si | O==O | Si—O |
| 键能(kJ·mol-1) | a | b | c |
(5)铁和氨气在640 ℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式


人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化、聚乙烯、二氧化硅等17种“分子”改变过人类的世界。
(1)Fe单质为体心立方晶体,晶胞中铁原子的配位数为_______________ ,基态铁原子有_______________ 个未成对电子,Fe3+的电子排布式为_______________ 。
(2)硝酸钾中NO3-的空间构型为_______________ ,写出与NO3-互为等电子体的一种非极性分子化学式_______________ 。
(3)6氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有_______________ 。

(4)下列说法正确的有_______________ (填字母序号)。
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯( )分子中有5n个σ键
)分子中有5n个σ键
d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b) kJ
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图2所示,写出该反应的化学方程式 _______________ ,若两个最近的Fe原子间的距离为s cm,则该晶体的密度是____________ g•mol-1。
(1)Fe单质为体心立方晶体,晶胞中铁原子的配位数为
(2)硝酸钾中NO3-的空间构型为
(3)6氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有

(4)下列说法正确的有
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(
 )分子中有5n个σ键
)分子中有5n个σ键d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b) kJ
| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网