单选题 适中0.65 引用3 组卷719
用0.1000mol/L的标准盐酸分别滴定20.00mL的0.1000mol/L氨水和20.00mL的0.1000mol/L氢氧化钠溶液的滴定曲线如图所示,横坐标为滴定百分数(滴定用量/总滴定用量),纵坐标为滴定过程中溶液pH,甲基红是一种酸碱指示剂,变色范围为4.4-6.2,下列有关滴定过程说法正确的是

| A.滴定氨水溶液当滴定分数为50%时,各离子浓度间存在关系:c( |
| B.滴定分数为100%时,即为滴定过程中反应恰好完全的时刻 |
| C.从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳 |
| D.滴定氨水溶液当滴定分数为150%时,所得溶液中离子浓度有大小关系c(Cl-)>c(H+)>c( |
2017·安徽·一模
类题推荐
25℃时,用0.1000mol/L的NaOH溶液分别滴定20.00mL浓度均为0.1000mol/L的CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法不正确的是

| A.点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH) |
| B.④⑤为两个反应的滴定终点,两个反应均可采用酚酞作指示剂 |
| C.点①溶液中水的电离程度小于点②溶液 |
| D.点②和点③间(不含端点)存在离子浓度大小关系:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
25℃时,用0.1000mol/L的NaOH溶液分别滴定20.00mL浓度均为0.1000mol/L的CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法不正确的是

| A.点①和点②所示溶液中:c(CH3COO﹣)﹣c(CN﹣)═c(HCN)﹣c(CH3COOH) |
| B.④⑤为两个反应的滴定终点,两个反应均可采用酚酞作指示剂 |
| C.HCN酸性比CH3COOH弱,所以点①溶液中水的电离程度小于点②溶液 |
| D.点②和点③间(不含端点)存在离子浓度大小关系:c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣) |
室温下,用0.1000mol/L盐酸分别滴定20.00mL浓度均为0.1000mol/L氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积V[HCl(aq)]的变化关系如图所示。下列说法不正确的是
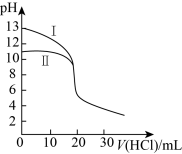
| A.Ⅱ表示是滴定氨水的曲线,V[HCl(aq)]=20mL时:c(Cl-)>c( |
| B.pH=7时,两种溶液中:c(Na+)=c( |
| C.滴定氢氧化钠溶液,V[HCl(aq)]>20mL时可能有c(Cl-)>c(Na+)>c(H+)>c(OH-) |
| D.滴定氨水时,当V[HCl(aq)]=10mL时,有2[c(OH-)-c(H+)]=c( |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


