解答题-实验探究题 适中0.65 引用1 组卷346
如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的离子反应方程式为:_____________ .装置 B 中饱和食盐水的作用是_________________ ;
若C处发生了堵塞,则B中的现象为__________________ .
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ应该依次放入____ (填编号)
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为______ 色,说明 ________________ ;打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是__________________ ;
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为_____ .
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用的漂白液,同时有 NaHCO3 生成,该反应的化学方程式是______ .
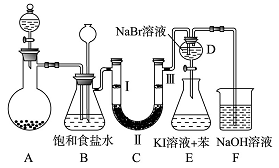
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的离子反应方程式为:
若C处发生了堵塞,则B中的现象为
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中Ⅰ、Ⅱ、Ⅲ应该依次放入
| ① | ② | ③ | ④ | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为
(4)如果将二氧化锰与足量的浓盐酸混合加热,若有17.4g 的 MnO2 被还原,则被氧化的 HCl 的质量为
(5)向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用的漂白液,同时有 NaHCO3 生成,该反应的化学方程式是
16-17高一下·辽宁葫芦岛·开学考试
类题推荐
下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
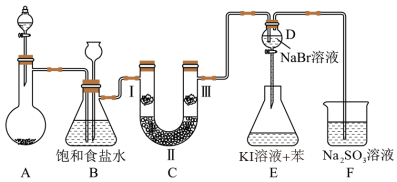
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的反应方程式为___________ ;装置B中饱和食盐水的作用是___________ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入___________ 。
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入一定通入一定量的氯气,可以看到无色溶液逐渐变为黄色,反应方程式___________ ,继续打开活塞,将装置D中少量溶液加入装置E中振荡,观察到的现象是___________ ;该现象___________ (填“能”或“不能”)说明溴的氧化性强于碘,原因是___________ 。

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的反应方程式为
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入一定通入一定量的氯气,可以看到无色溶液逐渐变为黄色,反应方程式
如图是某同学设计的制备少量氯气并进行系列实验的装置(夹持及加热仪器已略).
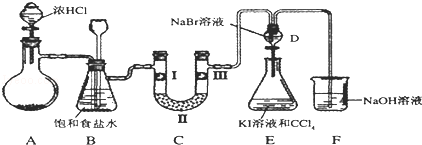
(1)若装置A中制备氯气选用的药品为固体二氧化锰和浓盐酸,请写出装置A中的化学反应方程式: ;
实验室也可用高锰酸钾制氯气:2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
该反应中的氧化剂是 ,若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是 mol;
(2)装置B中饱和食盐水的作用是 ;
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入 (填编号);(碱石灰为NaOH与CaO混合物,无水氯化钙为中性干燥剂)
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱.当向D中缓缓通入少量氯气时,可以看到D中无色溶液逐渐变为 色,若打开D装置的活塞,使D中溶液滴入E装置(KI溶液与CCl4),振荡锥形瓶后静置一会儿,可以观察到的现象是 ;
(5)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式 .

(1)若装置A中制备氯气选用的药品为固体二氧化锰和浓盐酸,请写出装置A中的化学反应方程式: ;
实验室也可用高锰酸钾制氯气:2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
该反应中的氧化剂是 ,若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是 mol;
(2)装置B中饱和食盐水的作用是 ;
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入 (填编号);(碱石灰为NaOH与CaO混合物,无水氯化钙为中性干燥剂)
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 无水氯化钙 | 碱石灰 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式 .
下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。

(1)固体二氧化锰和浓盐酸制备氯气的化学反应方程式为:__________________ 。装置B中饱和食盐水的作用是__________________ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________________ 。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入______ 。(填序号)
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为橙黄色,说明Cl2氧化性_________________ Br2(填>、<或=)。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是__________________________ 。
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式____________________ 。

(1)固体二氧化锰和浓盐酸制备氯气的化学反应方程式为:
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


