填空题 较易0.85 引用3 组卷502
(1)向某NaOH溶液中投入一块Al箔,先无明显现象,随后逐渐产生气泡,则产生气泡的离子反应方程式为______ 。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为______
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为______
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为____ 。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为
16-17高一上·安徽六安·期末
类题推荐
某课外小组探究钠、铝、铁、铜单质还原性强弱及其相关化学性质,做了如下实验:
(1)实验1中能发生反应的离子方程式______________________________________ 。
(2)实验2中能够判断出铝、铁、铜还原性强弱的现象是________________________ 。
结论:由实验1、2得出四种金属的还原性强弱顺序为______________ ;请从原子结构角度解释钠的还原性强于铝________________________________________ 。
(3)为确认实验2反应后溶液中的金属阳离子,再进行实验:
①取Al反应后的溶液加入过量的NaOH溶液,写出反应的离子方程式_______________ 。
②一段时间后,取Fe反应后的溶液,检验Fe2+方法正确的是__________________ 。
a.滴加KSCN溶液,无明显变化,再加入少量氯水,溶液变红
b.滴加K3[Fe(CN)6]溶液,有蓝色沉淀产生
c.滴加NaOH溶液,产生的白色沉淀迅速变成灰绿色,最终变成红褐色
(4)在实验2中,铝、铁反应现象的差异并不是很明显,有同学建议再设计一种实验来证明这两种金属的还原性关系,请设计一种实验方案___________________________ 。
(5)在实验过程中,还有同学为了验证铁与铜的还原性,用铁、铜、导线、烧杯、氯化铁溶液设计了原电池装置。
①画出原电池的装置图_________________________________________________ 。
②该电池的正极反应为_________________________________________________ 。
| 实验1 | 常温时取四种金属少量分别放入装有蒸馏水的试管中 |
| 实验2 | 再取少量铝、铁、铜分别放入装有稀硫酸的试管中 |
(2)实验2中能够判断出铝、铁、铜还原性强弱的现象是
结论:由实验1、2得出四种金属的还原性强弱顺序为
(3)为确认实验2反应后溶液中的金属阳离子,再进行实验:
①取Al反应后的溶液加入过量的NaOH溶液,写出反应的离子方程式
②一段时间后,取Fe反应后的溶液,检验Fe2+方法正确的是
a.滴加KSCN溶液,无明显变化,再加入少量氯水,溶液变红
b.滴加K3[Fe(CN)6]溶液,有蓝色沉淀产生
c.滴加NaOH溶液,产生的白色沉淀迅速变成灰绿色,最终变成红褐色
(4)在实验2中,铝、铁反应现象的差异并不是很明显,有同学建议再设计一种实验来证明这两种金属的还原性关系,请设计一种实验方案
(5)在实验过程中,还有同学为了验证铁与铜的还原性,用铁、铜、导线、烧杯、氯化铁溶液设计了原电池装置。
①画出原电池的装置图
②该电池的正极反应为
某研究小组利用如图所示的装置,进行CO还原Fe2O3的实验(固定装置略)。
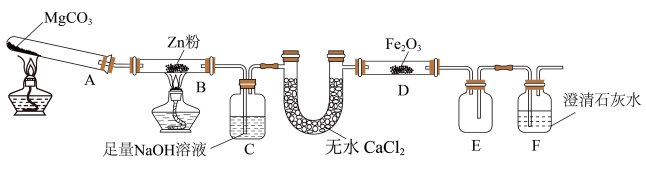
(1)装置B中发生的化学方程式________________ 。装置C的作用是__________________________
(2)用酒精喷灯对装置D加热,得到灰黑色粉末用黑色粉末进行以下实验:
①得到的灰黑色粉末是________________ (填写化学式)。
②步骤2中“白色沉淀最终变为红褐色”的化学反应方程式为_________________ 。
③步骤4中,溶液变红的原因为_____________________________________________________________ ;溶液褪色可能的原因______________________________________ ;验证上述原因的实验操作方法为____________ 。
(3)上述装置,从实验安全考虑,需要采取的改进措施是________ 。

(1)装置B中发生的化学方程式
(2)用酒精喷灯对装置D加热,得到灰黑色粉末用黑色粉末进行以下实验:
| 步骤 | 操作 | 现象 |
| 1 | 取灰黑色粉末加入稀硫酸 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加NaOH溶液后,在空气中,搅拌放置 | 白色沉淀最终变为红褐色 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水至过量 | 先变红,后褪色 |
②步骤2中“白色沉淀最终变为红褐色”的化学反应方程式为
③步骤4中,溶液变红的原因为
(3)上述装置,从实验安全考虑,需要采取的改进措施是
下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向AlCl3溶液中逐滴滴加氨水至过量 | 先产生白色沉淀后沉淀溶解 | Al(OH)3能与碱反应 |
| B | 向少量NaOH溶液中放入一小块未打磨的铝片 | 无明显变化 | Al与NaOH溶液不反应 |
| C | 向FeSO4溶液中滴加NaOH溶液 | 生成的白色沉淀迅速变成灰绿色,最终变成红褐色 | Fe(OH)2易被氧气氧化为Fe(OH)3 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应生成Fe2O3 |
| A.A | B.B | C.C | D.D |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


